
Jasmin Merdan / Getty Images
Key Takeaways
- Új vizsgálatok 128 olyan molekuláris célpontot azonosítottak, amelyek megcélozhatók a koronavírusok más sejtekbe történő terjedésének megakadályozására.
- A transzmembrán fehérje 41 B szintén kapcsolódik a Zika vírus vírusreplikációjának elősegítéséhez.
- E fehérje deaktiválása potenciálisan hasznos lehet vírusellenes terápiákban.
Miközben a COVID-19 vakcinát fényként üdvözlik a pandémia végén, egy NYU-s kutatócsoport készít egy B tervet. A folyóiratban megjelent két tanulmányuk eredményeiSejtazt mutatják, hogy a specifikus fehérjék gátlása megakadályozhatja a SARS-CoV-2 vírus replikációját és végső soron a COVID-19 fertőzések kiváltását.
COVID-19 vakcinák: Legyen naprakész arról, hogy mely vakcinák állnak rendelkezésre, kik kaphatják és mennyire biztonságosak.
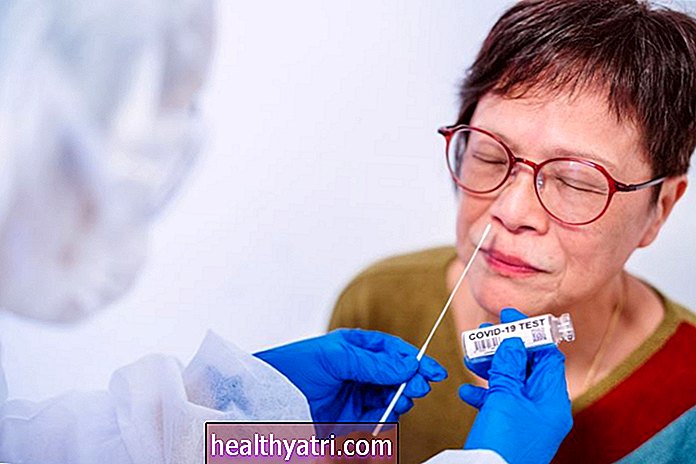
Hogyan okozhat fertőzést a SARS-CoV-2?
A vírusnak át kell adnia genetikai információit egy gazdasejtbe a szaporodás érdekében. Eric J. Yager, PhD, az Albany Gyógyszerészeti és Egészségtudományi Főiskola és a Biofarmáciai Oktatási és Képzési Központ mikrobiológiai docense azt mondja, hogy a vírusok nem rendelkeznek a saját fehérjék előállításához és a szaporodáshoz szükséges gépekkel. Ennek eredményeként az eltérítő sejtek túlélésükhöz szükségesek.
A SARS-CoV-2 tüskefehérjét használ az emberi sejtek felszínén található ACE2 receptorhoz való kötődéshez. A tüskefehérje kulcsként működik, amely az ACE2 receptorhoz kapcsolódik. Ez lehetővé teszi a vírus bejutását a sejtbe.
Annak érdekében, hogy az eltérítés sikeres legyen, Yager szerint a SARS-CoV-2 manipulálja a sejtet körülvevő védőréteget.
"A sejtmembránok sokféle lipidmolekulából állnak" - Yager, aki nem volt részese aSejttanulmányokat, mondja Verywell. "Ennek megfelelően a tudósok azt találták, hogy számos klinikailag releváns vírus képes megváltoztatni a gazdasejt lipid anyagcseréjét annak érdekében, hogy kedvező környezetet teremtsen a fertőző vírusrészecskék összegyűjtéséhez és felszabadulásához."
A vírus bejutva arra kényszerítheti a sejtet, hogy több másolatot készítsen róla. "A vírusok a gazdasejt gépezetét és bioszintetikus útjait választják a genom replikációjához és a vírus utódok termeléséhez" - mondja Yager.
A COVID-19 fertőzés megelőzése érdekében a kutatóknak meg kell akadályozniuk a vírus bejutását a sejtekbe.
A folyamatos koronavírus-kutatás a tüskefehérje blokkolására összpontosított. Valójában a Pfizer / BioNTech és Moderna által kifejlesztett COVID-19 mRNS vakcinák úgy működnek, hogy a sejteknek nem állandó utasításokat adnak a vírus tüskefehérjének ideiglenes létrehozására. Az immunrendszer felismeri a tüskefehérjét idegen betolakodóként, és gyorsan elpusztítja. A tapasztalat azonban lehetővé teszi az immunrendszer számára, hogy emlékezzen ezekre az utasításokra. Tehát, ha valódi vírus valaha bejut a szervezetébe, immunrendszere felkészítette a védekezéseket az ellene való harcra.
Bár a tüskefehérje jó célpont lehet, aSejttanulmány szerint nem ez az egyetlen.
"Fontos első lépés az új fertőzéssel szemben, mint például a COVID-19, a molekuláris táj feltérképezése, hogy megnézze, milyen lehetséges célpontokkal kell megküzdenie" - mondja John T. Poirier, PhD, az NYU Langone Health orvostudományi adjunktusa és a két tanulmány társszerzője egy friss sajtóközleményben. "Egy újonnan felfedezett vírus és más ismert vírusok összehasonlítása felfedheti a közös felelősségeket, amelyek reméljük, hogy a jövőbeni kitörések potenciális sebezhetőségének katalógusaként szolgálnak."
Egyéb potenciális célok vizsgálata
A kutatók arra törekedtek, hogy megtalálják az emberi sejtek molekuláris összetevőit, amelyeket a SARS-CoV-2 átvesz, hogy lemásolja önmagát. A CRISPR-Cas9 segítségével egyetlen gént inaktiváltak egy emberi sejtben. Összesen 19 000 gén működését kapcsolták ki. Ezt követően a sejteket SARS-CoV-2-nek és három másik koronavírusnak tették ki, amelyekről ismert, hogy közönséges megfázást okoznak.
A vírusfertőzés miatt sok sejt elpusztult. Az élő sejtek képesek voltak túlélni az inaktivált gén miatt, amelynek a szerzők szerint döntő fontosságúnak kell lenniük a replikáció szempontjából.
A kutatók összesen 127 olyan molekuláris utat és fehérjét találtak, amelyekre a négy koronavírusnak szüksége volt ahhoz, hogy önmagát sikeresen lemásolja.
Az azonosított 127 mellett a kutatók úgy döntöttek, hogy a transzmembrán fehérje 41 B-re (TMEM41B) koncentrálnak.
Döntésük egy 2016-os tanulmány információin alapult, amely azt mutatta, hogy a TMEM41B kulcsfontosságú volt a Zika vírus replikációjában. Bár ez a fehérje feladata a sejthulladék eltávolítása zsírbevonatba csomagolással, a kutatók szerint a koronavírusok képes legyen ezt a zsírt egyfajta rejtekhelyként használni.
Mit jelent ez az Ön számára
Amíg várunk egy nyilvánosan elérhető oltásra, a kutatók tovább fejlesztik a COVID-19 kezeléseket. A TMEM41B megcélzásával a tudósok képesek lehetnek olyan antivirális terápiák létrehozására, amelyek a súlyos betegségek megelőzésére összpontosítanak, megakadályozva a koronavírus terjedését a test többi részén.
Fehérjék célzása a gyógyszerfejlesztéshez
A vírusfehérjék megcélzása nem újszerű stratégia, mondja Yager. Bakteriális fertőzések kezelésében is működik.
"Az antibiotikumok, például a doxiciklin, a sztreptomicin és az eritromicin, megzavarják a 70S baktérium riboszómájának azon képességét, hogy szintetizálják a baktériumfehérjéket" - mondja Yager. "Az antibiotikumok, például a rifampicin, gátolják a bakteriális mRNS szintézisét, amelyet terveként használnak a baktériumfehérjék szintetizálására."
A kutatók úgy vélik, hogy a TMEM41B és más fehérjék potenciális célpontok lehetnek a jövőbeni terápiák során.
"Vizsgálataink együttesen jelentik a transzmembrán fehérje 41 B mint a flavivírusok fertőzésének kritikus tényezője, és figyelemre méltóan a koronavírusok, például a SARS-CoV-2 esetében is" - mondta Poirier sajtóközleményében. "Noha a transzmembrán fehérje 41 B gátlása jelenleg a legfőbb versenyző a koronavírus fertőzés megállítását célzó jövőbeli terápiákra, eredményeink több mint száz olyan fehérjét azonosítottak, amelyeket szintén lehetséges gyógyszeres célpontként vizsgálhatunk."



















-is-treated.jpg)

