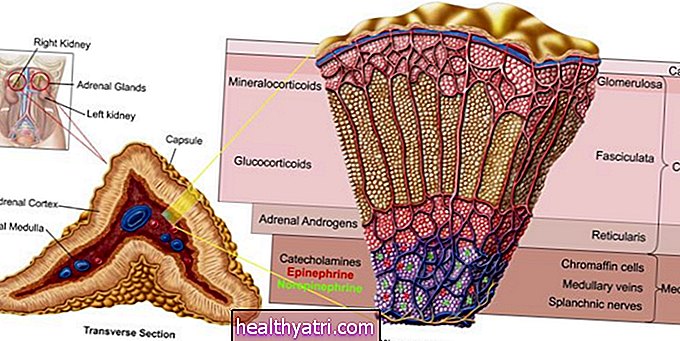
Az Országos Rákkutató Intézet a hisztopatológiát úgy határozza meg, hogy "a beteg sejtek és szövetek vizsgálata mikroszkóp segítségével". A szövettan a szövetek, a patológia pedig a betegség vizsgálata. Tehát együttvéve a hisztopatológia szó szerint azt jelenti, hogy a szöveteket tanulmányozzuk a betegségekkel kapcsolatban.
A hisztopatológiai jelentés leírja a vizsgálatra elküldött szövetet és annak jellemzőit, hogy miként néz ki a rák mikroszkóp alatt. A hisztopatológiai jelentést néha biopsziás vagy patológiai jelentésnek hívják.
Hős képek / Getty ImagesSzövettani jelentések
A szakorvost, aki mikroszkóp alatt végzi a vizsgálatot, patológusnak hívják. A vizsgált szövet biopsziából vagy műtéti eljárásból származik, amelynek során kiválasztják a gyanús szövet mintáját és elküldik a laboratóriumba.
Ezután feldolgozzák és nagyon vékony rétegekre (ún. Metszetekre) vágják, megfestik és mikroszkópokkal megvizsgálják a szövet sejtjeinek részleteit.
Egyes betegségek esetén a sebész fagyasztott metszetek alkalmazásával nagyon gyorsan értelmezheti a szövetmintát. A fagyasztott metszeteket vagy szeleteket takarékosan használják limfómában, az értelmezési és mintavételi problémák miatt.
Limfómákban a szövettanban a nyirokcsomók a leggyakrabban vizsgált szövetek. Számos vérráktípus esetén csontvelő biopsziára is szükség lehet a végleges diagnózis érdekében.
A hisztopatológiai jelentés elemei
A műtéti rákminták szövettani jelentései egyre bonyolultabbá válnak. Ezek a következőket tartalmazhatják:
- Az érintett szövet mikroszkópos megjelenése
- Különleges foltok
- Molekuláris technikák
- Egyéb vizsgálatok
A molekuláris technikák a sejtek és szövetek molekuláris szintű elemzésének képességére utalnak, amely a fehérjék, receptorok és az ezeket kódoló gének szintjén található.
A szövettani jelentés értelmezése
A szövetek ilyen vizsgálatának számos eredménye összefügg a prognózissal. A prognosztikai indikátorok magukban foglalhatják a tumor fokozatát és terjedésének mértékét, valamint azt, hogy a rákot eltávolították-e az egészséges sejtek körüli környezettel, vagy ha vannak bizonyítékok arra, hogy a rák túlterjedt az eltávolítottakon.
A besorolási rendszerek a besorolt rák fajtájától függően különböznek, de általában a sejteket az alapján osztályozzák, hogy milyen rendellenesek jelennek meg a mikroszkóp alatt, az 1. fokozatú daganatok normálisabb kinézetűek, a 4. fokozatú daganatok pedig több rendellenességet tükröznek.
A magas fokú daganat tehát általában olyan, amelyben a sejteknek több rendellenessége van. Az osztályozás nem azonos a színpadra állítással. A színpadképzésnek több köze van ahhoz, hogy a rák hol található a szervezetben, és milyen mértékben terjedt el.
Molekuláris leírások
A szövettani patológia mellett más módszerek is alkalmazhatók a rák jelenlétének felmérésére a szövetekben, ideértve a finom tűvel történő aspirációs citológiát is, és ezeknek a technikáknak egy része szélesebb körben alkalmazható az egész világon működő egészségügyi intézményekben.
A leukémiákat és a limfómákat megjelenésük kombinációjával diagnosztizálják:
- Citokémia: enzimek, amelyek lehetővé teszik bizonyos kémiai reakciók bekövetkezését
- Immunofenotípus: markerek vagy felületi fehérjék, amelyek antitest tesztekkel kimutathatók
- Kariotípus: kromoszómaváltozások
- Morfológia: a sejtek kinézete
Egyéb mintavételi technikák
A limfómákban és más rákos megbetegedésekben gyakran immunhisztokémia nevű technikát alkalmaznak a daganat típusának, prognózisának és kezelésének felmérésében.
Az immunhisztokémia magában foglalja az antitestek alkalmazását a ráksejtek külső oldalán lévő bizonyos címkékhez vagy markerekhez való tapadáshoz. Ezeknek a markereknek, amelyeken az antitestek ragaszkodnak, gyakran a nevükben "CD" van, ami a differenciálódás klaszterét jelenti.
Például a CD23 és a CD5 mikroszkopikus címkék, amelyek, ha jelen vannak a rákos sejtekben, alátámasztják azt az elképzelést, hogy a krónikus limfocita leukémia (CLL) / a kis limfocita limfóma (SLL) lehetséges diagnózis.
Ugyanezek a markerek más rosszindulatú daganatokban is jelen vannak, ezért az orvosok egyfajta eliminációs folyamatot alkalmaznak a rendelkezésre álló információk és a különféle rosszindulatú daganatokról, valamint azok "tipikus" CD-markerein alapuló ismeretek alapján.
A CD-marker másik példája a CD20, amely egyes limfómákban jelen van, másokban azonban hiányzik. A diffúz nagy B-sejtes limfóma vagy a DLBCL egy nagyon gyakori limfóma, amely a CD20 markerrel társul.
Egy adott leukémia- vagy limfómasejt-minta esetében a markereket egy teljes antitest-panel segítségével tesztelhetjük, amely beépül a pozitív és negatív kontrollokhoz különböző markerekhez.
Molekuláris és kromoszómális vizsgálatok végezhetők a gének átrendeződésének és a kromoszómák specifikus változásainak vizsgálatára. Néha a beillesztett vagy törölt gének összekapcsolódnak a prognózisra vonatkozó információkkal.
Például krónikus limfocita leukémia vagy CLL esetén a kromoszóma egy bizonyos része elvész, és gyakran elveszítik vele együtt a gént, amely segít elnyomni a rákot.
A 17p-deléció a CLL-ben szenvedő emberek körülbelül 5-10% -ában található meg. A 17p deléciójú CLL a CLL egy olyan formája, amelyet a hagyományos kemoterápiával nehezebb kezelni.












.jpg)