Az arzén-trioxid - más néven ATO vagy trisenox - az akut myeloid leukémia egyik altípusának rákellenes kezelése, akut promyelocytás leukémia vagy APL néven ismert. Ezt a leukémia altípust az akut mieloid leukémia „M3 altípusának” is nevezik.
Az újonnan diagnosztizált, alacsony vagy közepes kockázatú APL-ben szenvedő betegek kezelésében az ATO alkalmazásának eredményei nagyon kedvezőek voltak. Ezek a sikerek tudományos kutatást is ösztönöztek az ATO potenciális alkalmazásának vizsgálatára az APL-től eltérő számos rákban, ideértve a nem leukémiás rosszindulatú daganatos megbetegedéseket, például metasztatikus vastagbélrákot és az agydaganatot, a glioblastoma multiformát.
Az ATO-t gyakran kombinálják all-transz retinsavval (ATRA), egy retinoid ágenssel, amelyet az akut promielocita leukémia kezelésében használnak. A retinoid vegyületek megköthetik a sejtek receptorait, hogy fontos hatással legyenek a sejtek életciklusára. Az ATRA és az ATO kombinációja bebizonyosodott, hogy magasabb az ATRA és kemoterápiánál az újonnan diagnosztizált akut promyelocytás leukémia (APL) standard kockázatú betegek kezelésében.
Ariel Skelley / Getty Images
Hogyan működik az ATO?
Az ATO hatásmechanizmusát nem teljesen értik.
Az emberi promielocita leukémia sejtjeinek laboratóriumi vizsgálatai során az ATO változásokat okozott a sejtek megjelenésében, valamint a DNS töréseit - mindkettő az apoptózisnak vagy a programozott sejthalálnak nevezett folyamatot jelzi.
Az ATO emellett a promielocita sejtek által termelt fúziós fehérjét is károsítja, úgynevezett Pro-Myelocytic Leukemia / Retinoic Acid Receptor-alfa (PML / RAR alfa). A fúziós fehérjék két vagy több, különálló fehérjét kódoló gén összekapcsolódása útján létrejött fehérjék.
ATO az APL-hez
Az ATO-t az akut promyelocytás leukémia vagy az APL bizonyos eseteinek kezelésében engedélyezték, az alábbiak szerint:
- Újonnan diagnosztizált alacsony-közepes kockázatú APL, amelynek során az ATO-t all-transz-retinsavval vagy ATRA-val kombinálva alkalmazzák.
- Relapszusos / refrakter APL azoknál az embereknél, akiknek korábbi kezelése retinoidot és kemoterápiát tartalmazott, a rákos sejtekben bizonyos genetikai változások - a t (15; 17) transzlokáció és / vagy pro-myelocytás leukémia / retinsav jelenlétében. -receptor-alfa (PML / RAR-alfa) gén.
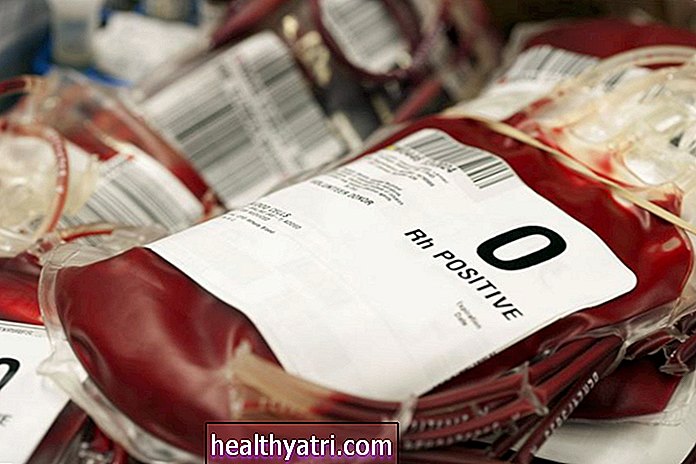
Egy személy fehérvérsejtszámát (WBC) a bemutatáskor, vagy az APL kezdeti értékelése és diagnosztizálása idején gyakran használják ezen APL kockázati csoportok létrehozására, ezáltal a következő kategóriákat használják:
- Alacsony vagy közepes kockázatú APL = kezdeti fehérvérsejtszám ≤10 000 / mikroL;
- Magas kockázatú APL = A kezdeti fehérvérsejtszám> 10 000 / mikroL.
Az ATO biztonságosságát és hatásosságát 17 éves korig nem igazolták. Az 5 évesnél fiatalabb gyermekekről nem állnak rendelkezésre adatok, az idősebb gyermekek esetében korlátozottak az adatok: egy elemzésben hét 18 év alatti (5-16 éves korú) beteget kezeltek ATO-val az ajánlott 0,15 mg / dózisban. kg / nap, és öt beteg teljes választ kapott.
A többi AML altípus ATO-ra adott válaszarányát nem vizsgálták. Az ATO-val kapcsolatos tanulmányok folyamatban vannak, és a jövőben ennek a szernek különféle további alkalmazásai lehetnek a rák kezelésében.
ATO + ATRA mint indukciós terápia
Az APL kezelése eltér az AML más típusaitól. Az indukciónak nevezett kezelés első lépése a remisszió megvalósítását célozza, és magában foglalja az APL kóros sejtjeinek, a promielocitáknak arra való kényszerítését, hogy normálisabb sejtekké növekedjenek.
Az all-transz-retinsav vagy az ATRA egy nem kemoterápiás gyógyszer, amelyet gyakran alkalmaznak indukcióra, mivel a rosszindulatú promielocitákat neutrofilekké érik. Ez egy olyan vegyület, amely rokon az A-vitaminnal. Az ATRA önmagában azonban általában nem elegendő a remisszió kiváltásának elvégzéséhez - vagyis önmagában az ATRA-val történő remissziók általában rövid életűek, csak néhány hónapig tartanak .
Így az ATRA általában más szerekkel kombinálva remissziót vált ki APL-ben szenvedőknél. Az ATRA antraciklin alapú kemoterápiával kombinálva az a standard kezelés, amelyre vonatkozóan a legszélesebb körű klinikai tapasztalat és a legtöbb adat áll rendelkezésre.
Nagy az érdeklődés azonban az ATO (ha van ilyen) ATRA-val történő használata iránt, a szokásos antraciklin alapú kemo helyett. Kezdetben ezt olyan lehetőségnek tekintették, akik nem tolerálták az antraciklin alapú kemoterápiát. A legfrissebb klinikai vizsgálatok adatai azonban azt sugallják, hogy az ATRA + ATO kombináció ugyanolyan jó eredményeket hozhat, ha nem is jobb, mint a szokásos sémák, amelyek kombinálják az ATRA-t a kemoterápiával - a megfelelő betegtípusokban.
Az ATRA + ATO adatok többsége olyan tanulmányokból származik, amelyekben az emberek alacsony kockázatú és közepes kockázatú APL-vel rendelkeztek; kevesebb információ áll rendelkezésre arról, hogy az ATRA + ATO hogyan viszonyulhat az ATRA + kemóhoz magas kockázatú APL-ben szenvedő betegeknél.
Konszolidációs terápiák
Az AML más típusaihoz hasonlóan az APL-ben szenvedő betegek további kezelést kapnak, méghozzá a kezdeti indukciós kezelés befejezése után, és ezt a későbbi kezelést konszolidációs terápiának nevezik.
Az alkalmazott specifikus gyógyszerrendek részben attól függnek, hogy milyen kezeléseket végeztek indukciós terápiaként. Példák a konszolidációs terápiákra:
- Antraciklin + ATRA néhány ciklusra (különböző ciklusokban különböző antraciklinek alkalmazhatók)
- Antraciklin + citarabin legalább 2 ciklusig
- ATO 2 cikluson keresztül, körülbelül 75 napig, majd ATRA + antraciklin 2 ciklusig
- ATRA plusz ATO több ciklusra
Karbantartási terápiák
Néhány APL-ben szenvedő beteg esetében a konszolidációt legalább egy évig fenntartó terápia követheti ATRA-val. Néha a kemo-gyógyszerek 6-merkaptopurin (6-MP) és metotrexát alacsony dózisát is adják.
ATO egyéb betegséghelyszínekhez - előzetes kutatás
Az APO-val az APL kezelésében elért sikerek tudományos érdeklődést váltottak ki az ATO potenciális szerepéről az egyéb rosszindulatú daganatok kezelésében.
Sok esetben a kutatás nagyon előzetes, időnként „kémcsövekre és állatkísérletekre” korlátozódik, azonban önmagában figyelemre méltó az a tény, hogy az ATO-t a legkülönbözőbb különböző betegségekben és helyeken vizsgálják.
E különböző kutatási irányok mintája következik.
A vastagbélrák tüdőmetasztázisai
Az örökbefogadó T-sejtes terápia az immunrendszer rákos megbetegedések és más betegségek elleni küzdelem elősegítésére szolgáló kezelés. A T-sejteket a betegtől összegyűjtik és a laboratóriumban növesztik, hogy maximalizálják a sikeres immunrendszeri válasz esélyét, majd visszateszik a betegbe a rák elleni küzdelem érdekében.
Wang és munkatársai egy állatkísérletben, amelyetOncotargetAz ATO citotoxikus T-sejtekkel kombinálva szinergetikus hatást és hosszabb túlélési időt mutatott a vastagbélrák tüdőmetasztázis-modelljében. Wang és kutatók megjegyezték, hogy az adoptív T-sejtes terápia sikerei gyakran a szabályozó T-sejtek redukciójának tulajdoníthatók, és hogy az ATO-nak pozitív hatása lehet e sejtek kimerítésével.
Májrák tüdőmetasztázisai
Tekintettel az ATO sikerére az APL-ben, a kutatók arra voltak kíváncsiak, vajon az ATO-nak lehet-e hasonló hatása a májrákban. Lu és munkatársai beszámolója szerint az ATO infúziói gátolják a tumor növekedését a májrákban.
Ezenkívül az ATO hatékony gyógyszer a májrákból származó tüdőáttétek és a kapcsolódó rákfájdalmak kezelésében.Lu és munkatársai megjegyezték, hogy a vizsgálatok kimutatták, hogy az ATO gátolhatja a májrák sejtjeinek invázióját és áttétjét az RhoC nevű fehérje gátlásával, és hogy a RhoC és annak „unokatestvérmolekulája”, az ezrin részt vehet az ATO tumorellenes funkciójában. .
Ezért arra törekedtek, hogy tanulmányozzák az áttétes májrák sejtek ATO általi gátlásának mechanizmusát. Megfigyelési ablakként az ezrin expressziós mintáit használták az ATO kezelés előtt és után, és azt találták, hogy az ATO kezelés jelentősen csökkentheti az ezrin expresszióját májrákban.
Glioblastoma multiforme
A Glioblastoma multiforme vagy GBM gyorsan növekvő, agresszív agydaganat. Ez a fajta rák ölte meg Ted Kennedy életét, és John McCain szenátort 2017-ben diagnosztizálták.
Az arzén-trioxidról beszámoltak arról, hogy klinikailag biztonságos dózisban (1-2 μM) gátolja, de nem visszafejli a szolid tumorok sokféle növekedését, beleértve a GBM-et is. Yoshimura és munkatársai megjegyezték, hogy az arzén-trioxid alacsony koncentrációja (2 μM) indukálhatja a GBM-sejtek differenciálódását, és fokozhatja más rákellenes terápiák hatását is, ha egérvizsgálatukban kombinációban alkalmazzák őket, és reméljük, hogy ez új lehetőségeket jelenthet a jövőbeli GBM-terápiákra.
Osteosarcoma
Az osteosarcoma gyakori csontrák, és a gyógyulási arányok az elmúlt 25-30 évben nem sokat mozogtak.
Az autofágia nevű folyamat arra utal, hogy a sejtek lizoszómái lebontják és eliminálják a fehérje aggregátumokat és a károsodott organellumokat - lényegében a szemetet kivéve a sejt citoplazmájának tisztán tartása érdekében.
Az autofágia-modulációt potenciális terápiás stratégiának tekintették az osteosarcoma esetében, és az előző vizsgálat azt mutatta, hogy az ATO jelentős anti-karcinogén aktivitást mutat.
Wu és munkatársai nemrégiben kimutatták, hogy az ATO fokozta az autofágia aktivitását a kísérleti humán osteosarcoma sejtekben (MG-63 sejtvonal). Érdekes, hogy az autofágia blokkolása (gyógyszerekkel vagy géntechnológiával)csökkentaz ATO által indukált sejthalál, ami arra utal, hogy az ATO kiváltja az autofág sejtpusztulást az MG-63 sejtekben.
Wu és munkatársai arra a következtetésre jutottak: „Összességében ezek az adatok azt mutatják, hogy az ATO túlzott autofágia indukálásával osteosarcoma sejtpusztulást vált ki, amelyet a ROS-TFEB útvonal közvetít. Ez a tanulmány az ATO-kezelés új, tumorellenes mechanizmusát nyújtja osteosarcomában. "
Egy szó Verywellből
Az elmúlt harminc évben az APL súlyos halálos betegségből nagyon gyógyíthatóvá vált. Az ATRA-val végzett kezelési stratégiákat, a kemoterápiát és újabban az ATO-t fontosnak tartják ezekben az előrelépésekben.
Ezekkel az előrelépésekkel azonban még mindig van néhány „rendezetlen terület”. Itt figyelembe vehető az ATO hosszabb távú biztonságossága és hatékonysága, bár az ATO + ATRA-val kapcsolatos, eddig jelentett hosszú távú adatok kedvezőek voltak. Egy másik rendezetlen terület lehet az, amely az ATRA / ATO korában az előnyben részesített fenntartó terápiák.



















.jpg)