Christoph Burgstedt / Science Photo Library / Getty Images
Key Takeaways
- Az emlőrák kemoterápiáján átesett emberek az egészséges sejtjeik és a rákos sejtjeik elpusztulásának mellékhatásával foglalkoznak.
- A jövőbeli rákterápiák megcélozhatók a rákkezelések hatékonyabbá és kevésbé károsakká tétele érdekében.
- Évente 325 000 emlőrákkal diagnosztizált ember közül csaknem 30 000 hordoz sajátos genetikai változatot, amely lehetővé tenné ráksejtjeik elpusztítását anélkül, hogy károsítaná normális sejtjeiket.
- A kutatók továbbra is meghatározzák a további célpontokat, amelyek növelnék azok számát, akik részesülhetnek a célzott rákterápiákban.
Új kutatások azt mutatják, hogy olyan új célzott terápiák fejleszthetők ki az emlőrák számára, amelyek nemcsak megállítják a sejtek növekedését a rákos sejtekben, hanem megölik azokat az egészséges sejtek károsítása nélkül. Bár a célzott terápiák nem új keletűek, ez a kutatás új célpontot is meghatároz annak meghatározása érdekében, hogy kik részesüljenek az e célt szolgáló jövőbeli terápiákból.
Mint minden rák, úgy az emlőrák is akkor kezdődik, amikor a normális, egészséges sejtek változásokon mennek keresztül, és olyan gyorsan osztódni kezdenek, hogy a sejtek növekedése nem kontrollálható. Az eredmény egy sejttömeg, amelyet csomóként éreznek. Az emlőrák diagnosztizálása után a kezelés gyakran kemoterápiát is magában foglalhat. De a kemoterápia kemény lehet, nemcsak a rossz rákos sejteket, hanem a jó egészséges sejteket is megöli, és a kemoterápián átesett embereket nagyon rosszul érezhetik. A jövőben lehetnek olyan kezelések, amelyek csak a rákos sejteket célozzák meg és megőrzik az egészséges sejteket, a rákkezelés hatékonyabbá és kevésbé ártalmasá tétele.
A Maryland-i Baltimore-i Johns Hopkins Egyetem Orvostudományi Egyetem és az Egyesült Királyság Oxfordi Oxfordi Egyetem tudósainak közös kutatásának eredményei azt mutatják, hogy a rákos sejtek megcélozhatók, majd elpusztíthatók a sejtosztódás szempontjából fontos enzim megszakításával. TanulmányukatTermészetszeptember 9-én.
"A sejtosztódás megcélzása logikus megközelítés a rákos sejtek elpusztításában, mivel a rák rendellenes sejtnövekedés, de a jelenlegi kezelések az egészséges sejteket is megölik" - írta a tanulmány szerzője, Andrew Holland, PhD, a Johns Hopkins Egyetem Orvostudományi Karának biológia és genetika docense. Baltimore-ban, mondja Verywell. "Például a Taxol (paclitaxel) rákkezelésével a csontvelőt és az őssejteket kiirtják, így a betegek gyengének érzik magukat, és hajhullást okoznak."
A sejtosztódás szerepe a rákban
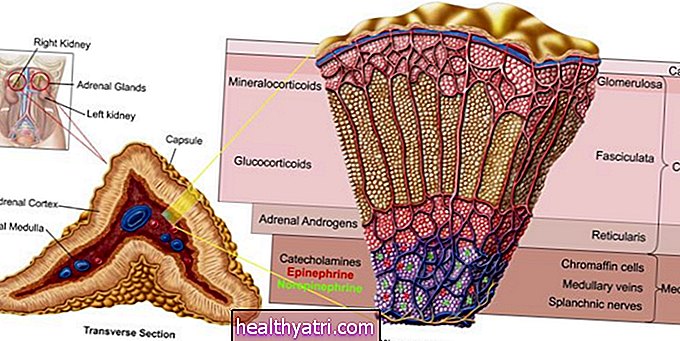
A sejtek öregedésével egy sejtosztódásnak vagy mitózisnak nevezett folyamat során pótolják magukat. A sejteken belüli egyik struktúra, az úgynevezett centroszóma, döntő szerepet játszik a sejtosztódásban, a sejtek megoszlásához a centroszómának meg kell duplikálnia önmagát. Miután ez megtörtént, a két centroszóma a sejt ellentétes végeire mozog. A fehérjék minden centroszómánál összegyűlnek, segítve a sejtek két leánysejtbe történő széthúzását. Amikor mutáció történik, a folyamat elromlik. A sejtosztódás túl gyakran történik, túl sok sejtet termel, és daganatot eredményez.
Rákölő stratégia
A rák kezelése magában foglalhatja a műtétet, a sugárzást és a hagyományos kemoterápiát, amely megöli a rákos sejteket és az egészséges sejteket is. Újabban a célzott terápiák váltak elérhetővé. Megkülönböztetőbb kezelések abban a tekintetben, hogy megcélozzák a rákos sejtek bizonyos részeit és megállítják növekedésüket, de bár nem ölnek meg egészséges sejteket, előfordulhat, hogy nem is ölik meg a rákos sejteket.
"A sejtosztódás már korábban is megcélzott volt, és sok gyógyszer megállíthatja, de ez a toxicitást eredményezi" - mondja a Wellwellnek William Cance, az amerikai ráktársaság orvosi és tudományos főtisztviselője, a grúziai Atlantában.
Például egy terápia célozhat egy rákos sejtben lévő fehérjét, de ugyanez a fehérje létezhet normális, egészséges sejtekben is. Tehát egy fehérjét célzó terápia a sejtosztódás során (úgynevezett anti-mitotikus célzott terápiák) megakadályozhatja a rákos sejtek duplikációját, de mérgező lehet az egészséges sejtekre is, mellékhatásokat okozva.
"Pontos mutációkat kell felfedezni és specifikusan megcélozni" - mondja Cance.
A rákos sejteket elpusztító, de a normális sejteket kímélő stratégiák azonosításához a kutatóknak meg kellett találniuk a rákos sejtek sebezhetőségét és ki kellett használniuk. És megtették.
Az 17q23 nevű genetikai variáns az emlőrákban szenvedő emberek 9% -ában található meg a sejtekben, és hatásának felerősítésével a TRIM37 nevű fehérjét aktívabbá teszi. Ha a TRIM37 aktívabb, a centroszómák nem viselkednek helyesen, és hibák lépnek fel a sejtosztódás során, ami a túlaktív sejtosztódáshoz vezet, amely daganatot eredményez.
A PLK4 nevű enzim elindítja a hibás sejtosztódási folyamatot a TRIM37-et túlzottan expresszáló sejtekben. A tanulmány kimutatta, hogy egy vegyi anyag alkalmazása a PLK4 enzim blokkolására megzavarta a centroszómákat, lényegében megölve a rákos sejteket, megakadályozva azok duplikációját.
"Ha eltávolítjuk ezeket a centroszómákat, a rákos sejtek nem tudnak életben maradni" - mondja Holland. "A sejtszintű változások ösztönözhetik az evolúciót, de a hibák lehetővé teszik a sejtek sebezhetőségét."
A terápia céljainak meghatározása
A rákos sejtek célzott megközelítéssel történő elpusztításához célokat kell meghatározni. "Ez potenciálisan új osztályokat és új típusú rákellenes szereket nyithat meg a jövőben" - mondja Cance.
"A TRIM37 gént túlzottan expresszáló emlőrákos betegek nagy része a 17q23 amplifikációját hordozza magában" - mondja Holland. "Feltétlenül képesek leszünk felhasználni a tanulmány eredményeit olyan tesztek kidolgozására, amelyekkel olyan embereket találhatunk meg, akik valószínűleg reagálnak egy adott terápiára."
Ezeknek a céloknak a felhasználása hasonló lesz ahhoz, amit jelenleg a daganatok tesztelésére tesznek az emlőrák altípusainak, például a HR- / HER2 + meghatározásához, vagy a családtagok genetikai vizsgálatához, hogy megnézzék, hordozzák-e a BRCA1 vagy BRCA2 gént vagy más örökletes mutációt.
"Az emlőrák HER2 + altípus a 17q23 amplikont hordozó rákok 40-50% -ával, valamint a BRCA1 és a tripla-negatív emlőrákok jó részével társul" - mondja Holland. "A 17q23 amplikon az összes emlőrák 9% -ában megtalálható - nagyjából ugyanaz, mint az összes BRCA-beteg együttvéve."
Ez azt jelenti, hogy évente 325 000 ember emlőrákot diagnosztizált, közülük körülbelül 30 000 részesülhet egy jövőbeni célzott terápiában, amely a 17q23, a TRIM37 és a PLK4 kölcsönhatásán alapul.
"Az izgalom itt egy nagyobb terápiás hatású kezelés miatt van, mert a toxicitás csak a rákos sejtekre korlátozódna" - mondja Holland.
Következő lépések
Ez az új tanulmány hozzájárul ahhoz az ismeretanyaghoz, amely elősegíti a speciális tesztek és a jövőbeni terápiák kidolgozását, de még korai. Mielőtt egy új kezelés a nyilvánosság számára elérhetővé válna, további feltáró vizsgálatokat kell elvégezni.Ha további laboratóriumi vizsgálatok pozitívnak tűnnek, klinikai vizsgálatokra van szükség a legjobb dózis meghatározásához, valamint a hatékonyság és a biztonság értékeléséhez. Ezután a kezelést az Élelmiszer- és Gyógyszerügyi Hivatal (FDA) szabályozási felülvizsgálatának és jóváhagyásának megköveteli. Mindez évek munkáját és kitartását igényli.
"A rákos sejtek rezisztenciát fejtenek ki olyan terápiákkal szemben, mint például a kináz (enzim) inhibitorok, például a PLK4. Ez az egyik legnagyobb probléma a rákban" - mondja Cance. "Ez a kutatás a normális sejteket megkímélő mechanizmusnak tűnik. A kihívás olyan kezelések kifejlesztése lesz, amelyek megakadályozzák, hogy a rákos sejtek újraprogramozzák kinázukat és tovább növekedjenek."
Cance szerint ez a tanulmány megnyitja a kaput különböző típusú célzott rákterápiák és új típusú rákellenes gyógyszerek számára, amelyek nem korlátozódnak az emlőrákra. A megkülönböztetőbb terápiák biztonságosabbá és hatékonyabbá teszik a rák minden típusának kezelését.
Mit jelent ez az Ön számára
Ha Önnek vagy szeretteinek emlőrákja van, ez a tanulmány reményt kínál a személyre szabott kezelésekre a jövőben. Tudja, hogy a kutatók szerte a világon keményen dolgoznak azon, hogy megtalálják az Ön állapotának legjobb célzását és kezelését.
Ha fennáll az emlőrák veszélye, beszéljen orvosával a kockázat csökkentéséről. Bár nem változtathatja meg génjeit vagy életkorát, éberen figyelhet az irányítható kockázati tényezők kezelésére, mint például:
- Az alkoholfogyasztás korlátozása
- A túlsúly csökkentése
- A dohányzás abbahagyása
- Elég testmozgás
- Havi mell-önvizsgálatok elvégzése












.jpg)