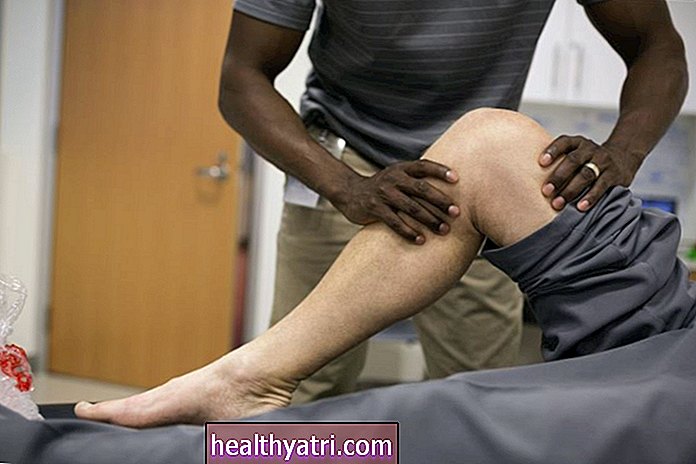
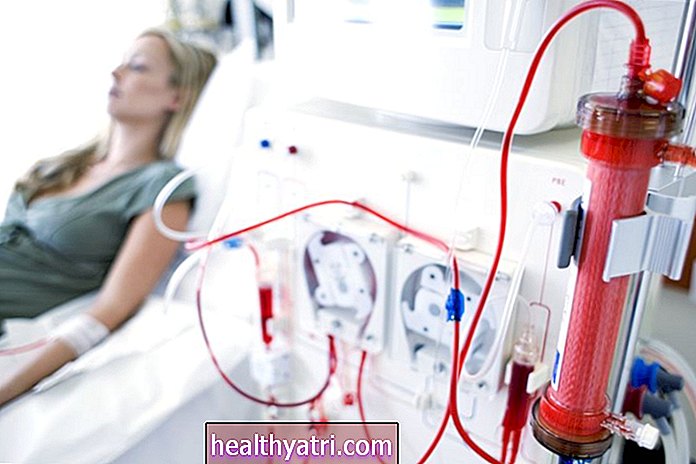
A Li-Fraumeni-szindróma vagy LFS genetikai állapot, amely hajlamosítja az egyéneket különböző rákos megbetegedésekre. Az LFS-ben szenvedő emberek gyakran az életkorban hamarabb fejlesztik ki ezeket a rákokat, mint az általános népességre jellemző. Nagyobb lehet a másodlagos vagy az azt követő rákos megbetegedések kockázata az LFS-ben.
A szindrómát először olyan családokban ismerték fel, amelyek életük elején sokféle rákot, különösen szarkómát fejlesztettek ki. Ezenkívül a családtagok nagyobb valószínűséggel fejlesztettek ki több új és különböző rákot egy életen át. Frederick Li és Joseph Fraumeni Jr voltak azok az orvosok, akik először 1969-ben jelentették ezeket a megállapításokat, és így kapta a nevét az LFS.
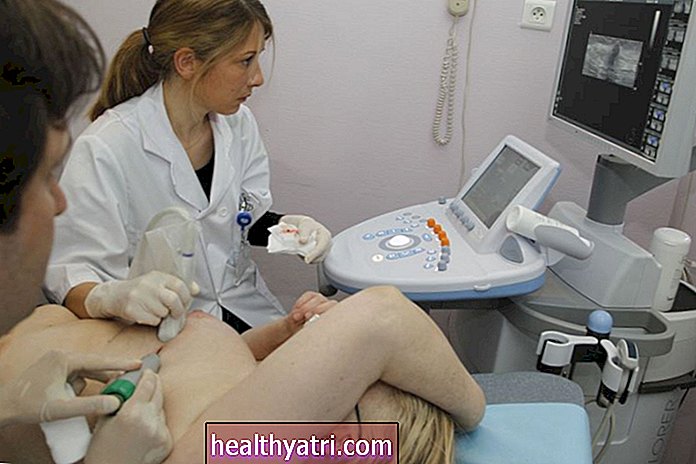
Hős képek / Getty ImagesMiért nagyobb a rákkockázat?
A Li-Fraumeni-szindrómában szenvedőknél nagyobb a rák kockázata, mert öröklődtek az úgynevezett csíra mutáció egy fontos génben, az ún.TP53.
A csíravonal mutáció olyan genetikai változás, amely az érintett egyén szüleinek csíravonalában következett be - vagyis a petefészkekben vagy a herékben lévő sejtekben kezdetben mutáció következik be, amelyek petesejtet és spermát eredményeznek. Ezekben a sejtekben található mutációk az egyetlen olyan mutációk, amelyek a fogamzás pillanatában közvetlenül az utódoknak átadhatók, amikor a petesejt és a spermium találkozik, és zigótát képeznek. Így a csíra mutációk hatással lesznek az új utód testének minden sejtjére; ezzel szemben a szomatikus mutációk valamikor az egyénben valahol kialakulnakutánvagy sokkal, de sokkal később, és változó számú sejtet érintenek a testben.
Az LFS-ben szenvedő családok legfontosabb csíravonal-mutációi azok, amelyek befolyásolják aTP53gén. A rákkutatás világában azTP53 a gén annyira kritikus, hogy „a genom őrzőjének” nevezték.
TP53 egy tumor szupresszor gén - vagyis egy olyan gén, amely megvédi a sejteket a rák felé vezető út egy lépésétől. Amikor ez a gén úgy mutálódik, hogy nem úgy működik, ahogy rendelték, vagy annak funkciója nagymértékben csökken, a sejt rákká fejlődhet, gyakran más genetikai változásokkal kombinálva. TeszteléseTP53 a csíravonal mutációit először 1990-ben fejlesztették ki, amikor megerősítették a kapcsolatot a p53 és az LFS között. Azóta közel 250 mutáció az egészTP53 gént kimutattak.
Egy másik gén, a hCHK2 mutációja is társult az LFS-hez; jelentősége azonban nem világos. A hCHK2 gén egy tumor szupresszor gén, amely a DNS károsodására reagál. Csak kevés család hordozza ezt a mutációt, és az érintetteknél hasonló a rosszindulatú daganatok köre, mint a TP53 mutációval rendelkezőknél.
Mennyire magas a kockázat?
Becslések szerint egy LFS-ben szenvedő embernek 40% -ig 50% -os, 60 éves koráig pedig 90% -os esélye van a rák kialakulására. Ha LFS-e van, akkor egyéni kockázata részben függ hogy férfi vagy nő-e, a nőknél általában nagyobb a kockázat, mint a férfiaknál.
Ha megnézzük az 50 éves korban LFS-ben szenvedő férfiak és nők életkori rákkockázatát, akkor a rák kialakulásának kockázata a következőképpen oszlik meg: nőknél 93%, férfiaknál 68%. Ha mégis rák alakul ki, a nők hajlamosak arra, hogy ezt a rákot is korábbi életkorban fejlesszék: átlagosan 29 év, szemben a férfiak 40 éves korával.
Mai és munkatársai tanulmánya szerint a nőknél a magasabb kockázat elsősorban a korán kezdődő emlőráknak köszönhető. Ezek a kutatók azt is megállapították, hogy a pozitív tesztet mutató nők körébenTP53mutációk, az emlőrák messze a leggyakoribb rosszindulatú daganat volt. A kumulatív emlőrák előfordulása körülbelül 85% volt 60 éves korig. Ugyanebben a tanulmányban az emlőrák kockázata jelentősen megnőtt egy nő 20-as éveiben, ami megerősítette, hogy a 20 éves kortól kezdődő emlőrák-szűrés jó gyakorlat LFS-ben szenvedő nőknél.
Ez a kockázati szint aTP53mutációk összehasonlíthatók a BRCA1 és BRCA2 csíravonal mutációval rendelkező nőknél tapasztaltakkal - olyan gének, amelyek a BRCA1 / 2 mutációk genetikai teszteléséről és a megelőző masztektómiákról szóló jelentések során (a hírességek, mint például Angelina Jolie) jelentőséget kaptak.
Melyek a magrákok?
Bármely rák bármikor kialakulhat. Azonban az LFS-ben szenvedő emberekről ismert, hogy korai rákdiagnózisuk van, és életük során nagy a kockázata a többféle „alapvető” ráknak, beleértve a következőket:
- Osteosarcoma - a rák leggyakoribb típusa, amely a csontokban kezdődik
- Lágyrész szarkómák - bizonyos típusú szövetekből, például zsírból, izomból, idegekből, rostos szövetekből, erekből vagy mély bőrszövetekből kialakuló rákfajta
- Korán megjelenő emlőrák
- Agydaganatok
- Leukémia - a vérképző sejtek rákja
- Mellékvese kérgi karcinóma - a mellékvese kéregének rákja, amely a mellékvesék külső rétege (a mellékvesék a vese tetején fekszenek, és fontos szerepet játszanak a különböző hormonális funkciókban)
Kleihues 1997-es tanulmányában az LFS-ben a leggyakrabban azonosított szarkóma az oszteoszarkóma volt, amely az esetek 12,6% -ának felel meg, ezt követi az agydaganatok (12%) és a lágyrész szarkómák (11,6%). A lágyrész szarkómák közül a rhabdomyosarcomákat azonosították leggyakrabban. Egyéb, ritkábban jelentett szarkómák közé tartoznak a fibrosarcomák (ami már nem tekinthető igazi entitásnak), atípusos fibroxanthomas, leiomyosarcomas, orbitális liposarcomas, orsósejtes szarkómák és differenciálatlan pleomorf szarkómák. Hematológiai daganatok vagy vérrákok (például akut limfoblasztos leukémia és Hodgkin-limfóma), valamint az adrenokortikális karcinómák 4,2%, illetve 3,6% gyakorisággal fordultak elő.
Mivel több olyan LFS-re jellemző genetikai mutációval rendelkező családot azonosítottak, sokkal több rákot vontak be.
Az LFS rák spektruma kibővült a melanoma, a tüdő, a gyomor-bél traktus, a pajzsmirigy, a petefészek és más daganatokkal.
A hagyományos értékelések alapján úgy tűnik, hogy a lágyrész-szarkóma és az agyrák kialakulásának kockázata a gyermekkorban a legnagyobb, míg az osteosarcoma kockázata a serdülőkorban lehet a legnagyobb, a női emlőrák kockázata pedig 20 éves kor körül jelentősen megnő, és idősebb korban is folytatódik felnőttkor. Ezek a statisztikák azonban változhatnak, mivel a rákra hajlamosító gének tesztelésének gyakorlata fejlődik.
Hogyan határozható meg a Li-Fraumeni-szindróma?
Ennek a szindrómának különböző kritériumai és definíciói vannak. Egyesek befogadóbbak, mint mások. A klasszikus LFS a legkorlátozóbb definíció, mivel 45 éves kor előtt szarkóma-diagnózist igényel, míg a későbbi meghatározások, például a Chompret-kritériumok, megpróbálják felhalmozni a daganattípusokról és az életkorukról a diagnózis diagnosztizálásakor.
Klasszikus LFS kritériumok:
- 45 éves kora előtt szarkómát diagnosztizálnak (ráktípus, amely magában foglalja az izom / csontváz / ízületek / zsír eredetű sejteket) és
- Van egy első fokú rokona (szülő, testvér vagy gyermek), akinek bármilyen rákja van diagnosztizálva 45 éves és annál fiatalabb életkor előtt
- Van még egy első vagy másodfokú rokona (beleértve a nagynéniket, nagybácsikat és még sok más), akinek 45 éves kora előtt diagnosztizált rákja van, vagy bármely életkorban diagnosztizált szarkóma van.
Li-Fraumeni-szerű (LFL) kritériumok:
- Az LFL-kritériumok szélesebb hálót vetnek be más ráktípusokra, és tartalmaznak néhány rokont, akiket 45 éves kor után diagnosztizáltak, és két különböző definíció van használatban:
- Nyír definíció: bármilyen gyermekkori rákot vagy szarkómát, agydaganatot vagy mellékvesekéreg-karcinómát diagnosztizálnak 45 éves kora előtt, és első vagy másodfokú rokona tipikus Li-Fraumeni rákkal rendelkezik (szarkóma, emlőrák, agydaganat, adrenokortikális karcinóma vagy leukémia) bármely életkorban, és első vagy második fokú rokonuk bármilyen rákos megbetegedéssel rendelkezik 60 éves kor előtt.
- Az angolna definíciója: Két első vagy másodfokú rokona van Li-Fraumeni-val összefüggő rosszindulatú daganatokban (szarkóma, emlőrák, agytumor, leukémia, mellékvese-daganat, melanoma, prosztatarák, hasnyálmirigyrák) bármely életkorban.
Chompret kritériumok:
- A Li-Fraumeni tumor spektrumához tartozó daganata van (lágyrész szarkóma, osteosarcoma, premenopauzális emlőrák, agydaganat, adrenocorticalis carcinoma, leukémia vagy bronchoalveolaris tüdőrák) 46 éves kora előtt, és legalább egy első vagy második - rokon Li-Fraumeni daganattal (kivéve az emlőrákot, ha mellrákja van) 56 éves kor előtt, vagy több daganattal vagy
- Több daganata van (a több emlődaganat kivételével), amelyek közül kettő a Li-Fraumeni daganat spektrumához tartozik, és az első 46 éves vagy
- Adrenocorticalis carcinoma vagy choroid plexus tumor diagnosztizálva van, függetlenül a család előzményeitől.
Az LFS Schneider és munkatársai által végzett áttekintése szerint a klinikailag diagnosztizált egyének legalább 70% -ánál (vagyis a fenti definíciókat használva) azonosítható káros csíravonal-mutáció van.TP53tumor szupresszor gén.
A rák kezelése
Ha egy LFS-ben szenvedő egyénnél rák alakul ki, rutinszerű rákkezelés ajánlott, kivéve az emlőrákot, amelyben a lumpectomia helyett mastectomia ajánlott a második emlőrák kockázatának csökkentése és a sugárterápia elkerülése érdekében.
Az LFS-ben szenvedőknek javasoljuk, hogy a másodlagos sugárzás okozta rosszindulatú daganatok kockázatának korlátozása érdekében, amikor csak lehetséges, kerüljék a sugárterápiát. Ha azonban a sugárzást orvosilag szükségesnek tartják az adott rosszindulatú daganatból való túlélés esélyének javításához, akkor azt a kezelőorvos és a páciens belátása szerint fel lehet használni.
Szűrés és megfigyelés
Egyre többször szólítják fel a szakértőket, hogy konszenzust alakítsanak ki arról, hogy miként kell átvizsgálni és gondozni az FLS-ben szenvedő családokat. Sajnos, bár a tudomány gyorsan fejlődik, még nem létezik ilyen konszenzus minden területen.
A gyakorisága károsTP53 mutációk az általános populációban és az FLS valódi gyakorisága nem ismert. A becslések 5000-ből 1 és 20 000 között változnak. Ahogy több család megy átTP53tesztelés során az LFS valódi prevalenciája egyértelműbbé válhat.
Az emlőrák kockázatának kezelése
Az Egyesült Államokban a National Comprehensive Cancer Network (NCCN) irányelvei éves mell-MRI-t javasolnak azoknak, akiknek FLS-je 20-29 év közötti, és éves MRI-t és mammográfiát 30-75 év között. Ausztráliában a nemzeti irányelvek kétoldalú mastectomia felajánlását javasolják; egyébként az éves mell-MRI ajánlott 20-50 év. Schon és munkatársai azt javasolják, hogy fontolóra vegyék a kockázatcsökkentő bilaterális mastectomia vagy mellszűrés lehetőségét azoknál a nőknél, akiknél aTP53 gén.
NCCN ajánlások
Azon megállapítás alapján, hogy az emlőrák kockázata a második évtized után jelentősen megnő, az ajánlások között szerepel, hogy a bilaterális mastectomiát 20 éves kortól kell figyelembe venni. Az éves mellrák kockázata 40–45 év körüli csúcspontra esik, majd csökken, így a bilaterális mastectomia kevésbé valószínű, hogy a 60 év feletti nőknek kedvez.
- Melltudatosság, 18 éves kortól kezdve, periodikus, következetes mellvizsgálattal.
- Klinikai mellvizsgálat, 6–12 havonta, 20 éves kortól kezdődően
- 20–29 év, éves mell-MRI szűrés kontrasztdal
- 30–75 éves kor, éves mell-MRI szűrés kontraszt és mammogram segítségével, a Tomosynthesis figyelembevételével
- Életkor> 75 év, a kezelést egyénileg kell mérlegelni.
- A nők számára aTP53emlőrák miatt kezelt mutáció esetén, akiknek nem volt kétoldali mastectomia, az éves mell-MRI-vel és mammográfiával végzett szűrést a fent leírtak szerint kell folytatni.
- Amikor a kockázatcsökkentő mastectomia lehetőségét megvitatják, tanácsot kell adni a védelem mértékéről, az életkorra jellemző rák kockázatának mértékéről, a rekonstrukciós lehetőségekről és más rákok versengő kockázatairól. Az ilyen megbeszélésekbe be kell vonni a kockázatcsökkentő mastectomia pszichoszociális, társadalmi és életminőségi szempontjait.
Az egyéb rákkockázatok kezelése
NCCN ajánlások
- Átfogó fizikai vizsga, ideértve a neurológiai vizsgálatokat is, magas gyanakvási indexgel ritka rákos megbetegedések és daganatos túlélők második rosszindulatú daganatai miatt 6–12 havonta.
- Kolonoszkópia és felső endoszkópia 2–5 évente, 25 éves kortól kezdve, vagy 5 évvel a család legkorábbi ismert vastagbélrákja előtt (amelyik előbb bekövetkezik).
- Éves bőrgyógyászati vizsgálat 18 évtől kezdődően.
- Éves teljes test MRI
- Az éves agyi MRI elvégezhető az egész testre kiterjedő MRI részeként vagy külön vizsgaként.
A szűrés és a megfigyelés egyéb formái
Volt egy kísérlet a pozitronemissziós tomográfia (FDG-PET) / CT-vizsgálatokról LFS-ben szenvedő felnőtteknél, amely 15 egyén közül háromban mutatott ki daganatot. Ezek a PET-CT-vizsgálatok, jóllehet bizonyos daganatok megtalálására kiválóak, minden alkalommal növelik a sugárterhelést, ezért ez a szkennelési módszer leállt, és áttért az egész test MRI-re felnőtteknél.TP53káros változatok.
Számos kutatócsoport intenzív szűrőprogramot kezdett alkalmazni, amely magában foglalja az egész testre kiterjedő gyors MR-vizsgálatot, az agyi MRI-t, a hasi ultrahangvizsgálatot és a mellékvesekéreg működésének laboratóriumi vizsgálatát. Ez a fajta megfigyelési program javíthatja az LFS-ben szenvedők túlélését azáltal, hogy bármilyen tünet nélkül felismeri a daganatokat, de további vizsgálatokra van szükség annak bizonyítására, hogy ez a fajta kezelés működik LFS-ben szenvedő felnőtteknél és gyermekeknél.
Az LFS-ben szenvedő egyéneket megkérdezték a rákfelügyelethez való hozzáállásukról, és úgy tűnik, hogy a legtöbb hisz abban, hogy a daganatok korai stádiumban történő felderítése értéket jelent. Beszámoltak a rendszeres megfigyelési programban való részvétellel kapcsolatos kontroll és biztonság érzéséről is.
Gyermekek tesztelése TP53 mutációkra
Lehetséges a gyermekek és serdülők tesztelése az LFS jellegzetes mutációi tekintetében, de kérdéseket vetettek fel ennek lehetséges kockázataival, előnyeivel és korlátaival kapcsolatban, beleértve a bizonyított felügyeleti vagy megelőzési stratégiák hiányát, valamint a megbélyegzéssel és a diszkriminációval kapcsolatos aggályokat.
Javasolt, hogy teszteljék a 18 évesnél fiatalabb személyeketTP53 a kórokozó-variánsokat olyan programon belül kell elvégezni, amely mind a teszt előtti, mind a teszt utáni információkat és tanácsadást biztosítja.