Noha a dohányzás továbbra is a tüdőrák fő oka, amely az összes tüdőrákos eset 80-90% -áért felelős, az örökletes egyes esetekben hozzájárulhat a tüdőrák kialakulásához. Becslések szerint a tüdőrák 8% -a genetikai hajlam: A tüdőrák kockázata megnőhet, ha egy szülő vagy testvér megbetegedik; még így sem jelenti azt, hogy biztosan megkapja a betegséget, ha a családjában másnak van.
A jelenlegi kutatások szerint a genetika nagyobb valószínűséggel járul hozzá a tüdőrákhoz azok számára, akik:
- Fiatal (50 év alatti)
- Női
- Soha nem dohányzók
A tudósok azonosítottak bizonyos genetikai mutációkat (változások a genetikai kódban), amelyek növelhetik a tüdőrák kockázatát. De ez nem jelenti azt, hogy a tüdőrákhoz kapcsolódó összes genetikai mutáció öröklődik. Örökölheti a genetikai mutációkat, vagy ezeket a változásokat életében bármikor megszerezheti környezeti tényezők (például dohányzás vagy szennyezés) következtében.
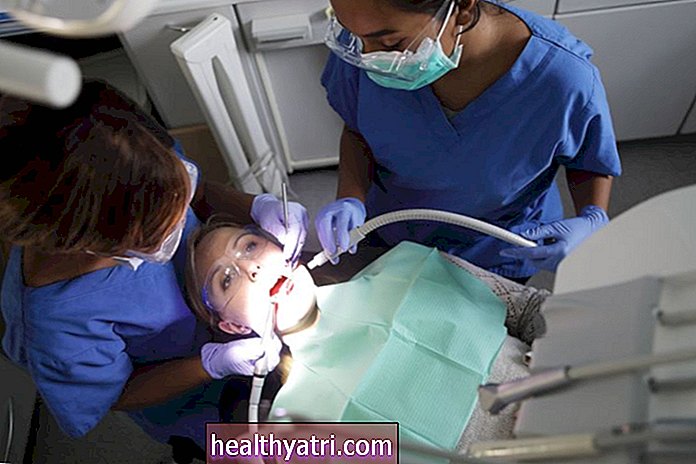
JR Bee illusztrációja, Verywell
Befolyásoló tényezők
Családtörténet önmagában nem tudja megjósolni, hogy tüdőrák lesz-e vagy sem. A családi tüdőrák olyan kifejezés, amely arra utalhat, hogy a rák génje „átkerül” a szülőktől a gyermekek felé.
Ma a kutatók a családi tüdőrákot akombinációgenetikai és környezeti tényezők, amelyek növelik a tüdőrák kockázatát a családtagok körében.
Összességében elmondható, hogy az első fokú rokon (szülő, testvér vagy gyermek) tüdőrákban szenvedő egyéneknek kb. 1,5-szer nagyobb a betegség kockázata, mint a családi kórtörténet nélkül. Ez igaz a dohányzókra és a soha nem dohányzókra is.
A dohányzás előzményei szinte mindig lényegesen hozzájárulnak a tüdőrák kockázatához, mint a betegség örökletes hajlamai.
A jelenlegi bizonyítékok arra utalnak, hogy a tüdőrák családi kockázatát több egymást keresztező tényező befolyásolja, többek között:
- Átöröklés
- Hasonló életmód (például dohányzás és diéta)
- Hasonló környezetek (például beltéri és kültéri levegőszennyezés)
Az otthoni passzív dohányzás például 20-30% -kal növelheti az ember tüdőrák kockázatát. Hasonlóképpen az otthoni radon-expozíció - az Egyesült Államok második legfontosabb tüdőrákos oka - szintén befolyásolhatja egy személy családi kockázata a betegségben.
Mint ilyen, a tüdőrák családi kórtörténetében nem lehet annyira megjósolni a betegség valószínűségét, mint rávilágítani a módosítható kockázati tényezők kiigazításának szükségességére, és fokozott figyelemmel kísérésre a tüdőrák bármely jele vagy tünete esetén.
A genetikai kockázatok bizonyítékai
Számos tényező utal egy kis örökletes komponensre, ha a tüdőrák kockázatáról van szó.
Fiatalabb kor
Az Egyesült Államokban az átlagos életkor, amikor a tüdőrákot diagnosztizálják, 70 év. Ennek ellenére vannak olyan emberek, akiknél jóval korábban diagnosztizálták a tüdőrákot. Valójában az összes tüdőrákos esetek körülbelül 1,3% -a 35 év alatti embereknél fordul elő.
Ennek a fiatalabb populációnak az az érdekes, hogy kevesen dohányoznak, ami kérdéseket vet fel, hogy mely egyéb tényezők járulhatnak hozzá a kockázat kialakulásához. Azoknál az embereknél, akiknél fiatalabb korban alakul ki tüdőrák, nagyobb valószínűséggel vannak genetikai változások a betegséggel kapcsolatban.
De ezeknek a genetikai változásoknak örökletes kapcsolatát nem sikerült megállapítani.
A fiatal felnőttek szinte mindegyik tüdőrákja adenokarcinoma, egyfajta rák, amely szorosan kapcsolódik bizonyos megszerzett (nem öröklött) genetikai mutációkhoz.
Szex
A férfiak és a nők körülbelül ugyanolyan valószínűséggel alakulnak ki tüdőrákban. Ennek ellenére vannak különbségek a nemek között.
A nők nemcsak a férfiaknál, hanem a férfiaknál is nagyobb valószínűséggel fejlődnek ki tüdőrákban, mint az férfiak, de ugyanolyan kockázati tényezőkkel rendelkező férfiaknál is.
A 2019-es felülvizsgálat szerintTranszlációs tüdőrákkutatás,azoknak a nőknek, akiknek a csomagolásának 40 éves múltja dohányzik, háromszor nagyobb a tüdőrák kockázata, mint az azonos dohányzási nyilvántartással rendelkező férfiaknál.
A genetikai vagy hormonális tényezők szerepet játszhatnak, valószínűleg növelhetik a nők biológiai érzékenységét a dohányfüstben található rákkeltőkre (rákot okozó szerekre).
Számos tanulmány kimutatta, hogy a nők magasabb koncentrációban tartalmazzák az úgynevezett CYP1A1 enzimet, amely mérsékelheti a szervezet reakcióját a rákkeltő anyagokra a tüdőben, és elősegítheti a rák kialakulását. Bizonyos genetikai polimorfizmusok (variációk) a CYP1A1 termelésének szabályozatlanságához kapcsolódnak, és megmagyarázhatják, hogy a nők miért vannak kiszolgáltatottabbak az inhalációs rákkeltő anyagokkal szemben.
Verseny
A faj és az etnikai hovatartozás szintén megkülönböztető tényező a tüdőrák kockázatában. A folyamatban lévő Felügyeleti, Epidemiológiai és Végeredmény Program (SEER) adatai megjegyzik, hogy az afroamerikaiaknál sokkal nagyobb a tüdőrák kockázata, mint bármely más faji vagy etnikai csoportnál.
A SEER adatai a különböző csoportok tüdőrák előfordulási arányát szolgáltatták (a 100 000 emberre eső esetek számában leírva):
- Fekete: 76,1 / 100 000
- Fehérek: 69,7 / 100 000
- Amerikai bennszülöttek: 48,4 / 100 000
- Ázsiai / csendes-óceáni szigetlakók: 38,4 / 100 000
- Spanyolok: 37,3 / 100 000
Bár a dohányzás és a környezet minden bizonnyal hozzájárul ehhez az arányhoz, a tudósok azt is megjegyezték, hogy a tüdőrákhoz kapcsolódó genetikai mutációk fajonként is változhatnak.
A jövőbeni tanulmányok meghatározhatják, hogy ezek a mutációk mennyiben járulnak hozzá a különböző fajok és etnikumok közötti kockázathoz, és hogy a genetikai mutációk öröklődnek-e vagy megszerezhetők-e.
Génmutációk
A tüdőrák egyes típusai szorosabban kapcsolódnak specifikus genetikai mutációkhoz, mint mások, de nem bizonyultak örökletesnek. Valójában úgy gondolják, hogy megszerezték őket. Ezek a mutációk megváltoztathatják a sejtek működését és életciklusát, kórosan és kontroll nélkül replikálódhatnak, ami a rák kialakulásához vezet.
A tudósok bizonyos genetikai mutációkat azonosítottak a karcinogenezissel (a rák kialakulásával) kapcsolatban a tüdőben. Ezeknek a mutációknak a túlnyomó része nem kissejtes tüdőrákhoz (NSCLC), főleg tüdő adenokarcinómához kapcsolódik, szemben a kissejtes tüdőrákkal (SCLC).
A tüdőrákhoz kapcsolódó genetikai mutáció nem jelenti azt, hogy tüdőrákot kap. A magas kockázatú egyénekben az emlőrák valószínűségének előrejelzéséhez használt BRCA mutációktól eltérően nincs genetikai mutáció vagy teszt, amely megjósolhatná avalószínűségtüdőrák.
EGFR
Az EGFR gén mutációi megváltoztathatják az epidermális növekedési faktor receptor nevű fehérje termelését, amely elősegíti a sejtek megfelelő reakciót a környezetükre. Nem kevesebb, mint 10 EGFR-mutáció ismert, amelyek tüdőrákhoz kapcsolódnak; még sokan várhatók azonosításra. A
A kutatások szerint az NSCLC-vel rendelkező ázsiaiak 47% -ának van EGFR-mutációja. A közel-keleti vagy afrikai származású NSCLC-s betegek körülbelül 21% -a szintén hordozza a mutációt; ugyanez igaz az európai származású betegek 12% -ára.
Az EGFR mutációk a nőknél és a nem dohányzóknál is gyakoribbak. Míg az EGFR mutációk főleg a tüdő adenokarcinómáihoz kapcsolódnak, egyesek agresszívebbé tehetik a laphámsejteket.
Az EGFR mutációk azonosíthatók mind az elsődleges (eredeti) daganatban, mind az áttétekben (távoli helyekre terjedő másodlagos daganatok). Ezek a mutációk általában gyorsan mutálódnak, és gyakran rezisztenssé válnak a kezelésükre alkalmazott gyógyszerekkel szemben.
KRAS
A KRAS gén felelős a K-Ras nevű jelátviteli fehérje termeléséért, amely utasítja a sejteket a felosztás, érés és működés működésére. Ennek a fehérjének a szabályozatlansága rákhoz vezethet.
A tüdő adenokarcinómában szenvedők kb. 15-20% -a pozitívnak bizonyítja a KRAS mutációkat. Ezek gyakran az EGFR mutációk mellett fordulnak elő.
A KRAS mutációkat elsősorban az elsődleges daganatban, ritkábban metasztatikus daganatokban azonosítják.
ALK
Az anaplasztikus lymphoma kináz (ALK) gén felelős egy olyan típusú tirozin-kináz fehérje termeléséért, amely utasítja a sejteket osztódásra és növekedésre. A pontosabban ALK-átrendeződésnek nevezett mutáció az NSCLC-hez kapcsolódik, és az ázsiaiaknál gyakrabban észlelhető, mint bármely más csoport.
Az ALK átrendeződése az NSCLC esetek 3–5% -ához kapcsolódik (főként adenokarcinómákhoz), és gyakrabban figyelhető meg könnyű dohányosok, nem dohányzók és 70 év alatti emberek körében.
BRCA2
Megállapították, hogy a BRCA2 génmutációval rendelkező emberek, amelyek az emlőrákhoz kapcsolódó mutációk egyike, nagyobb kockázattal járnak a tüdőrák kialakulásában is.
Ez a mutáció az európai származású emberek nagyjából 2% -ában található meg, és autoszomális domináns mintázatban öröklődik (ez azt jelenti, hogy csak egy szülőnek kell hozzájárulnia a mutációhoz a betegség kockázatának növelése érdekében).
A BRCA2 mutációval rendelkező dohányosok csaknem kétszer nagyobb eséllyel kapnak tüdőrákot, mint az általános populáció. Ezzel szemben a nem dohányzók, akiknek BRCA mutációja van, mérsékelten megnövekedett kockázattal rendelkeznek.
Az ezt a mutációt hordozó dohányosoknál leggyakrabban laphámrák alakul ki. A tüdő légutaiban pikkelysmr-karcinómák alakulnak ki, szemben a tüdő külső szélein kialakuló adenokarcinómákkal.
Szűrés és kezelés
A tudósoknak még sokat kell tanulniuk a tüdőrák genetikájáról. Bár egyértelmű összefüggések vannak a tüdőrák és az EGFR, KRAS, ALK és BRAF mutációk között, úgy vélik, hogy ezek a mutációk megszerzettek, és csak a rákos sejtekben találhatók meg, a test más sejtjeiben nem. Tehát a tüdőrák kialakulása előtt nem azonosíthatók (de bizonyos örökletes mutációk, például a BRCA1 és a BRCA2 előre azonosíthatók).
Jelenleg nincsenek ajánlások a tüdőrák genetikai szűrésére vonatkozóan. A tüdőrákhoz vezető vagy arra hajlamosító öröklődő gének azonosítására irányuló kutatási eredmények még mindig nem szolgáltatnak végleges információt.
A genetikai vizsgálatok segíthetnek a tüdőrák kezelésére szolgáló célzott terápiák kiválasztásában. Az ilyen típusú megközelítéssel a tüdőrák szövetét genetikai mutációk szempontjából tesztelik, és alkalmazható olyan rákkezelés, amely kifejezetten elpusztítja azokat a rákos sejteket, amelyek rendelkeznek az azonosított génmutációval.
Ezek a gyógyszerek specifikus kezelhető mutációkkal célozzák meg és elpusztítják a rákos sejteket, a normális sejteket nagyrészt érintetlenül hagyva. Emiatt a célzott terápiák gyakran kevesebb mellékhatást okoznak.
Az NSCLC-hez EGFR mutációval használt célzott gyógyszerek közül:
- Gilotrif (afatinib)
- Iressa (gefitinib)
- Tagrisso (ozimertinib)
- Tarceva (erlotinib)
- Vizimpro (dacomitinib)
Az NSCLC-hez ALK-átrendeződéssel alkalmazott célzott gyógyszerek közül:
- Alecensa (alektinib)
- Alunbrig (brigatinib)
- Lorbrena (lorlatinib)
- Xalkori (crizotinib)
- Zykadia (ceritinib)
Egy szó Verywellből
Ha nagy a kockázata a betegségnek, részesülhet a tüdőrák éves CT-szűréséből. Az éves szűrővizsgálatot jelenleg azoknak az 50 és 80 év közötti embereknek ajánlják, akik dohányoznak vagy leszoktak az elmúlt 15 évben, és legalább 20 csomagévnyi dohányzással rendelkeznek.
További kockázati tényezőktől függően, mint például a családi kórtörténet vagy a radon-expozíció, Ön és orvosa dönthet úgy, hogy ezeken a paramétereken kívül választja a szűrést. Ezzel korán elkaphatja a tüdőrákot, miközben még mindig nagyon kezelhető.



















.jpg)


