Az akut myeloid (vagy mielogén) leukémia (AML) altípusok egyre jobban megértésre kerülnek, új kutatási lehetőségek feltárásával. Az AML személyenként nagyon eltérő, és a prognózis gyakran gyenge. Ez döntő fontosságúvá teszi azokat a kutatásokat, amelyek elősegíthetik a túlélési arány javítását.
Az elmúlt évek új fejleményei javítják a diagnosztikát, a kezeléseket és a túlélési arányokat, amelyek mind reményteljesebb kilátást nyújtanak.
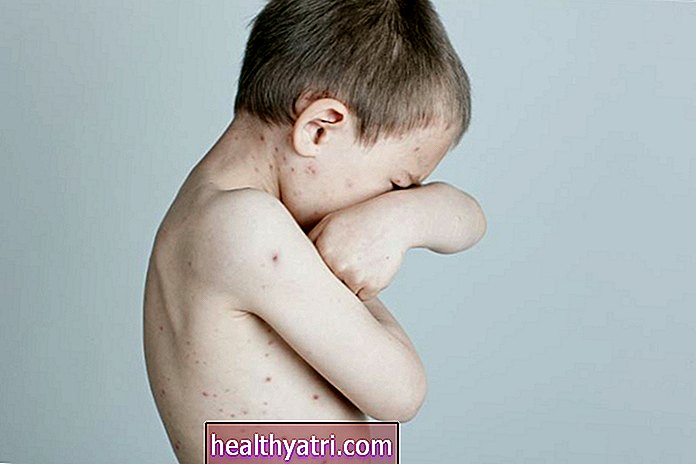
Az AML a vér és a csontvelő rákja (a csontok szivacsos belseje, ahol vérsejtek készülnek). "Akut", mert gyorsan halad. A "myeloid" azt jelenti, hogy myeloid sejteket foglal magában, amelyek különféle típusú vérsejtekké fejlődnek (például vörös és fehérvérsejtekké, vérlemezkékké).
Albina Gavrilovic / Getty Images
Az AML tünetei a következők:
- Láz
- Csontfájdalom
- Letargia és fáradtság
- Gyakori fertőzések
- Könnyű sérülés
- Szokatlan vérzés
Altípusok és színpadkép
Amikor a legtöbb rákot diagnosztizálják, akkor "szakaszosak". A szakasz megmondja, mennyire előrehaladott a rák, meghatározza a prognózist és irányíthatja a kezelési döntéseket.
Az AML nincs megrendezve. Ehelyett a kilátások és a kezelés az altípustól függ, amelyet laborvizsgálatok határoznak meg.
A legtöbb AML altípust részben az határozza meg, hogy a fejlett és rendellenes rákos sejtek mikroszkóp alatt néznek ki a betegség első diagnosztizálásakor. Ezenkívül az AML besorolást most kiegészítik az érintett genetikai változásokkal vagy mutációkkal kapcsolatos új felfedezések.
Két AML osztályozási rendszert használnak jelenleg:
- A francia-amerikai-brit (FAB) osztályozás
- Az Egészségügyi Világszervezet (WHO) osztályozása
A komplex genetikai altípusok szerinti további osztályozás fejlődik, köszönhetően a 2016-ban közzétett úttörő tanulmánynak.
Miért számít az altípus?
A leukémia genetikai összetételének ismerete segíthet orvosának megjósolni, hogy a jelenlegi kezelések hatékonyak-e. Ez a diagnózis rutinjának idején már kiterjedtebb genetikai vizsgálatokat végzett.
Az altípusok megértése szintén segíthet a kutatóknak új klinikai vizsgálatok megtervezésében az AML-típusok legjobb kezeléseinek kidolgozásában.
Az AML altípusok osztályozása
A FAB osztályozási rendszer az 1970-es évek óta létezik, de az altípusozási folyamat az elmúlt években párszor megváltozott. A WHO osztályozási rendszere 2008-ban vált szabványossá, csoportosítva az embereket a rákjuk hátterében álló genetikai változások alapján (ún. "Vezető mutációk").
Aztán 2016-ban sarkalatos kutatások jelentek meg aNew England Journal of Medicine (NEJM)ami még tovább vitte az altípust.
Ez a tanulmány bebizonyította, hogy a WHO molekuláris osztályozása az AML-esetek csaknem felénél nem működik jól - a vizsgálatban résztvevők 48% -át nem lehetett osztályozni a WHO molekuláris csoportjai alapján, pedig 96% -uknak voltak vezető mutációi.
A nyomozók a kezdetektől kezdve átértékelték az AML genomikus osztályozását, a következők alapján:
- Sok új leukémia gén felfedezése
- Több vezető mutáció felfedezése betegenként
- Komplex mutációs minták
Az AML FAB osztályozása
Több mint 40 évvel ezelőtt egy francia, amerikai és brit leukémia-szakértők egy csoportja az AML-t M0-M7 altípusokra osztotta annak alapján, hogy milyen típusú sejtből alakul ki a leukémia, és mennyire érettek a sejtek.
- Az M0 - M5 mind a fehérvérsejtek éretlen formáiban indulnak el.
- Az M6 a vörösvérsejtek nagyon éretlen formáiban indul ki.
- Az M7 a vérlemezkéket képző sejtek éretlen formáiban indul ki.
A WHO az AML osztályozása
A FAB osztályozási rendszert továbbra is gyakran használják az AML altípusokba csoportosítására; az ismeretek azonban előrehaladtak azon tényezők tekintetében, amelyek befolyásolják az AML különböző típusainak prognózisát és kilátásait.
Ezen előrelépések egy része tükröződött az Egészségügyi Világszervezet (WHO) 2008-as rendszerében, amely az AML-t több csoportra osztja:
- AML myelodysplasiaval kapcsolatos változásokkal
- A korábbi kemoterápiával vagy sugárzással kapcsolatos AML
- Myeloid szarkóma (más néven granulocita szarkóma vagy kloróma)
- Down-szindrómával kapcsolatos myeloid proliferációk
- AML kromoszóma transzlokációval és inverzióval
- AML nincs másképpen meghatározva
- Differenciálatlan és bifenotípusos akut leukémia
Az 5., 6. és 7. csoport tovább bontásra kerül.
AML kromoszómális transzlokációkkal és inverziókkal
Kromoszómális transzlokációk során a genetikai anyag egy része elszakad eredeti helyétől, és újból egy másik kromoszómához kapcsolódik. Az inverziókban egy szegmens kijön, fejjel lefelé fordul, és újra az eredeti kromoszómához kapcsolódik.
Az AML legalább hét típusa tartalmaz transzlokációkat, inverziókat vagy hasonló genetikai rendellenességeket.
Az AML nincs külön megadva
Az AML esetei, amelyek nem tartoznak a fenti csoportok egyikébe, a FAB rendszerhez hasonlóan vannak besorolva.
Differenciálatlan és bifenotípusos akut leukémia
Ezek leukémiák, amelyek mind limfocita, mind mieloid tulajdonságokkal rendelkeznek. Néha hívják őket:
- Akut limfocita leukémia (ALL) mieloid markerekkel
- AML limfoid markerekkel
- Vegyes akut leukémia
Új osztályozások: Az NEJM tanulmány
A közelmúltbeli változást kiváltó 2016-os tanulmányban 1540 AML-es ember vett részt. A kutatók 111 olyan gént elemeztek, amelyekről ismert, hogy leukémiát okoznak, azzal a céllal, hogy azonosítsák a betegség kialakulásának hátterében álló „genetikai témákat”.
Megállapították, hogy a résztvevőket legalább 11 fő csoportba lehet osztani, amelyek mindegyike különböző genetikai változási klaszterekkel rendelkezik, és eltérő a betegség jellemzői és jellemzői.
A tanulmány szerint a legtöbb embernek genetikai változások egyedülálló kombinációja volt a leukémiában, ami segíthet megmagyarázni, hogy az AML túlélési aránya miért változik nagyban. Így a kutatók ezen új információk felhasználásával új AML osztályozási rendszer kidolgozásán dolgoztak.
Arra a következtetésre jutottak, hogy három alcsoport létezik, amelyeket nem vettek figyelembe a WHO osztályozási rendszerében. Hívják őket:
- Chromatin-spliceosome
- TP53-aneuploidia
- IDH2R172
A javasolt rendszer használata az 1540 vizsgálat résztvevőjének osztályozásához:
- 1236 vezető mutációval rendelkező embert egy-egy alcsoportba lehet sorolni
- 56 beteg megfelelt két vagy több alcsoport kritériumainak
- 166 vezetői mutációval rendelkező ember maradt osztályozatlan
A szerzők azt javasolták, hogy rövid távon öt specifikus genetikai típust (úgynevezett TP53, SRSF2, ASXL1, DNMT3A és IDH2) építsenek be a prognosztikai irányelvekbe, mert ezek közösek és erősen befolyásolják az eredményeket.
Prognosztikai vs. Diagnosztikai
Az NEJM kutatói két külön osztályozási rendszert szorgalmaztak:
- Az egyik az emberek diagnosztizálásához használható
- Az egyik az eredmények (prognózis) előrejelzésére használható
Szerintük a diagnosztikai rendszernek fix tulajdonságokon kell alapulnia, míg a prognosztikai rendszernek a rendelkezésre álló kezelések alapján rendszeresen változnia kell.
Újabb kutatások
Nagyrészt az NEJM tanulmány alapján más kutatók az AML egyes genetikai profiljait vizsgálták. A 2020-ban közzétett tanulmányok szerint néhány kutató a következőket állapította meg:
- Lehetséges új korai diagnosztikai módszerek bizonyos altípusokra
- Lehetséges új módszerek a kábítószer-rezisztens emberek azonosítására
- A gyógyszerekkel szemben rezisztens esetek lehetséges új kombinációi
Egy tanulmány azonosított egy új gyógyszert, amely a kutatók szerint hatékony a gyógyszerrezisztens AML altípusok ellen, és használatuk után "azonnali klinikai hatással jár".
Az AML altípusok diagnosztizálása
Az orvosoknak rengeteg eszközük van az AML diagnosztizálására és az altípus meghatározására. A diagnózis fizikai vizsgálattal kezdődik. A vizsga során olyan jeleket keresnek, mint:
- Kiterjedt véraláfutás
- Vérzés
- Fertőzés
- A szem, a száj, a máj, a lép vagy a nyirokcsomók rendellenességei
Az AML gyanújának diagnosztizálásához a következő tesztek bármely kombinációját rendelhetik el:
- Teljes vérkép (CBC)
- Csontvelő törekvés
- Csontvelő biopszia
- Ágyéki szúrás
- Képalkotó tesztek (pl. Röntgen, CT vizsgálat, MRI)
- Citogenetika
A citogenetika és a molekuláris tesztek különösen fontosak az altípus meghatározásához. Magában foglalja a sejt genetikai anyagának mikroszkóp alatt történő vizsgálatát, hogy megtalálják a genetikai rendellenességeket, például transzlokációkat és inverziókat.
A leukémia diagnosztizálásaAltípusok és AML kezelés
Az Élelmiszer- és Gyógyszerügyi Hatóság az elmúlt években rengeteg új AML-gyógyszert hagyott jóvá; mindazok azonban jóval a 2016-os kutatás megjelenése előtt fejlesztés alatt álltak.
Most, nagyrészt e kutatás alapján, jelenleg számos lehetséges kezelést vizsgálnak az AML kezelésére specifikus genetikai altípusok alapján.
Számos, bizonyos genetikai mutációkat megcélzó vizsgálati gyógyszer megkezdte a kutatási folyamatot, és a kutatók új típusú kemoterápiás gyógyszereket, gyógyszer- és antitest-kombinációkat, valamint kinázinhibitoroknak nevezett gyógyszereket is vizsgálnak.
Ezen gyógyszerek egy része már más körülmények között is piacon van, míg mások ígéretes eredményeket mutatnak a vizsgálatok során. Például:
- A TET2 nevű AML mutáció lehetséges kezelése magában foglalhatja a PARP inhibitoroknak vagy HMA-knak nevezett gyógyszereket C-vitaminnal kombinálva.
- A KAT-nak nevezett enzimek csoportja segíthet az AML kezelésében az EP300 és CBP nevű gének mutációival.
- A p300 aktivátoroknak nevezett gyógyszereket az AML állatmodelljeiben vizsgálják.
Számos más AML genetikai altípust vizsgálnak, hogy a kutatók kideríthessék, milyen gyógyszerek célozhatják meg őket.
A leukémia kezelési lehetőségeiEgy szó Verywellből
Az akut myeloid leukémia mindig is félelmetes diagnózis volt, rossz kilátásokkal.
Azonban a rendelkezésre álló új gyógyszerek, az út közbeni út és a genetikai altípusok folyamatos új felfedezése révén a prognózis javul, és valószínűleg továbbra is így lesz.











-method.jpg)