Thana Prasongsin / Getty Images
Key Takeaways
- A sarlósejtes betegségnek csak egy FDA által jóváhagyott kezelése van, de ehhez testvér donor szükséges.
- A CRISPR-CAS9 technológia segítségével a kutatók sikeresen megcélozták azt a genetikai kapcsolót, amely kikapcsolta a hemoglobin magzati formájának termelését.
- A CRISPR-CAS9 lehetővé tette, hogy a sarlósejtes betegségben és a béta-thalassémiában szenvedő betegek saját donoruk legyenek a csontvelő-transzplantáció során. Ez lehetővé teszi a kezelések szélesebb körű hozzáférhetővé tételét.
A génszerkesztés számos tudományterületet feljavított, a peszticidektől mentes ételek létrehozásától a gyapjas mamut visszahozatali kísérleteig. A CRISPR-CAS9 nevű technológia, amelyet általában CRISPR-nek neveznek, a tudósok most megpróbálják kijavítani a betegségeket okozó genetikai hibákat.
Januárban megjelent januári tanulmányA New England Journal of Medicinemegállapította, hogy a CRISPR új kezeléseket kovácsolhat a vérbetegségek, például a sarlósejtes betegség gyógyítására.
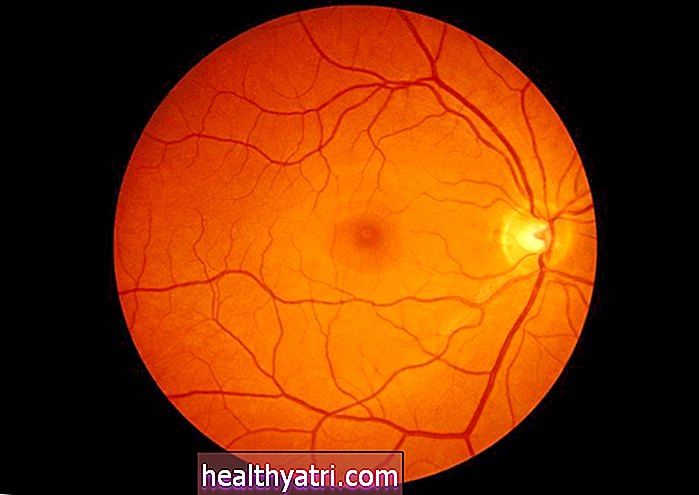
A sarlósejtes betegségben diagnosztizált betegeknél mutáció mutatkozik a hemoglobin - a vörösvértestekben vasban gazdag fehérje - génjében. A mutáció kórosan C alakú vérsejteket okoz, amelyek nehezen szállítják az oxigént a test más részeibe. Kemény és ragadós tulajdonsága eltömíti a véráramlást is, ami növeli a fertőzések kockázatát.
A sarlósejtes betegség egy örökletes vérbetegség, amely évente körülbelül 100 000 amerikait érint, mondja a Verywellnek Alexis A. Thompson, MD, MPH, az Amerikai Hematológiai Társaság egykori elnöke és a Feinberg Orvostudományi Kar gyermekgyógyászati hematológusa. Míg Thompson, aki nem vett részt a vizsgálatban, azt mondja, hogy a gyermekek születésükkor viszonylag normálisnak tűnnek, a gyermekek csak 6–12 hónapos korukban kezdenek problémákat kialakulni.
"A fiatalabb korosztályban a fájdalommal, súlyos lázzal vagy fertőzéssel jelentkező betegek kórházi kezelést igényelnek, nagyon erős gyógyszereket kapnak, és kimaradnak az iskolából" - mondja Thompson. "A felnőttkor felé haladva kihívásokkal küzdenek az oktatás, az egyetem befejezése és vagy munkahely fenntartása. ” A CRISPR segítségével a kutatók megpróbálnak változtatni ezeken az eredményeken.
Mit jelent ez az Ön számára
Az sarlósejtes betegség akkor terjed át a gyermekre, ha mindkét szülőnek van sarlósejt-vonása. Ha nem biztos a szállító státuszában, elengedhetetlen, hogy egészségügyi szakember átvizsgálja. Ha valóban sarlósejtes betegségben szenved, a jövőben új, CRISPR technológiát alkalmazó kezelések állhatnak az Ön rendelkezésére.
A genetikai stratégia újraindítja a hemoglobin termelést
A tanulmány egy sarlósejtes és egy béta-thalassemiában szenvedő beteget követett, amely vérbetegség csökkenti a hemoglobin termelését.
Mindkét betegnek szüksége volt vér őssejtekre, de a vizsgálat célja a sejtjeik használata volt, nem pedig egy testvér sejtjei. Amikor a vérből őssejteket vettek ki a pácienstől, a kutatók a molekuláris ollóként működő CRISPR-t és az egyvezető RNS-molekulát, a CAS9-et használták fel a BCL11A nevű specifikus gén felkutatására.
Ebben a tanulmányban a kutatók azért vágták le a BCL11A-t, mert genetikai kapcsolóként működik, amely kikapcsolja a hemoglobin magzati formáját előállító gént. A visszakapcsolásával a tudósok újra aktiválták a magzati hemoglobin termelését, amely mindkét beteg vörösvértestében pótolta a hiányzó vagy hibás hemoglobint. A megmaradt beteg sejteket kemoterápiával távolították el.
A kezelés után a hemoglobinszint stabil hónapokig megmaradt
A beavatkozás után hat és 12 hónappal mindkét beteg csontvelő-aspirátumokon esett át, hogy megmérje a csontmintában lévő vörösvérsejtek számát.
Az első beteg egy 19 éves nő volt, akinek diagnosztizálták a béta-thalassemiát. Négy hónappal a génnel szerkesztett őssejtekkel végzett utolsó csontvelő-átültetése után hemoglobinszintje stabilizálódott és stabil maradt az utolsó utólagos látogatásakor. Bár kezdetben súlyos mellékhatásokat tapasztalt a kezelésből (tüdőgyulladás és májbetegség), néhány hét múlva megszűntek.
A második beteg egy 33 éves nő volt, sarlósejtes betegségben. Tizenöt hónappal a beavatkozás után a magzati hemoglobinszintje 9,1% -ról 43,2% -ra emelkedett. Sarlósejtes betegségből származó mutált hemoglobinszintje 74,1% -ról 52,3% -ra csökkent. Míg három súlyos mellékhatást tapasztalt (szepszis, kolelithiasis és hasi fájdalom), kezeléssel megoldódtak.
Ennek a megközelítésnek az egyik fő előnye, szemben a vérbetegségek kezelésének hagyományos formáival, az, hogy a beteg sejtjeit donor nélkül igényli.
"Ugyanazon páciens sejtjei manipulálhatók és átültethetők az elutasítás veszélye nélkül, vagy immunreakciókat okozhatnak a donortól (graft-versus-host betegség)" - Damiano Rondelli, MD, Michael Reese, az egyetem hematológiai professzora a Chicago Orvostudományi Főiskolán Illinois-ból.
A publikálás óta a kutatók további nyolc betegre bővítették munkájukat - hat béta-thalassemiás és három sarlósejtes betegségben szenvedő betegre. Jelenlegi eredményeik összhangban vannak a vizsgálat első két betegével.
A sarlósejt-betegség jelenlegi kezelése
A sarlósejtes betegség FDA által jóváhagyott jelenlegi kezelése csontvelő-transzplantáció. Ehhez az eljáráshoz azonban szükséges, hogy a páciensnek legyen testvére, akinek a szövete tökéletesen megfelel az övéinek.
Thompson szerint a kezelés egyik fő kihívása az, hogy minden negyedik testvér nem azonos típusú szövet. Még akkor is, ha a csontvelő transzplantációra kerül sor, az eljárásnak súlyos mellékhatásai is vannak, beleértve a graft meghibásodását, a graft versus host betegséget és a halált.
Ha a csontvelő-transzplantáció nem szerepel a képen, akkor alternatív kezelésként egy haploid azonos transzplantációt alkalmazunk. "Sikert arattunk a haploid azonos transzplantációkkal, ahol a szövet típusa részben megegyezik, de az átültetést egészen más módon hajtják végre, hogy a szövődményeivel a beültetést elérhessük" - mondja Thompson. Szerinte azonban csak a betegek kisebbsége jogosult erre a kezelésre.
A sarlósejtes betegségre vonatkozó korlátozások és korlátozások miatt Thompson szerint volt némi vita arról, hogy a betegeket saját donorként szolgálják-e. Ebben a jelenlegi tanulmányban a szerzők a génszerkesztést tekintik az ilyen típusú kezelés lehetséges útjának.
Hogyan segíthetnek a genetikai kezelések
Bárki örökölheti a sarlósejtes betegséget, de különösen gyakori:
- Afrikai származású emberek, köztük afro-amerikaiak
- Spanyol-amerikaiak Közép- és Dél-Amerikából
- Közel-keleti, ázsiai, indiai és mediterrán származású emberek
Az Egyesült Államokban az országban született összes gyermeket átvizsgálják a sarlósejtes betegségben, ami bőséges lehetőséget biztosít a korai kezelésre. De több forgatókönyv kihívást jelent minden eset diagnosztizálására. Thompson szerint az Egyesült Államokba bevándorolt családoknak lehetnek olyan idősebb gyermekeik, akiket nem vizsgáltak át olyan szülőkkel együtt, akik nincsenek tisztában a szállítói státusukkal, amíg nincs gyermekük, akinek ilyen állapotban van.
A szűrések hiányosságai ellenére az iparosodott országok javították a sarlósejtes betegség prognózisát. "Ma egy, az Egyesült Államokban ma született gyermek 95% -os esélye van a felnőttkorban való túlélésre, és ugyanez vonatkozik más találékony országokra, például az Egyesült Királyságra" - mondja Thompson.
Globális szempontból azonban Thompson szerint az alacsony és közepes jövedelmű országok nem biztos, hogy ugyanazokat a kezeléseket kínálják, mint amelyek jelenleg elérhetők az olyan országokban, mint az Egyesült Államok.Szerinte a sarlósejtes betegségben szenvedő gyermekek több mint fele Afrika szubszaharai országában nem éli túl az ötödik születésnapját.
A tanulmány eredményei alapján a génszerkesztés elősegítheti a sarlósejtes betegségek kezelésének szélesebb körű hozzáférhetőségét.
"A remény az, hogy ez a kezelés hozzáférhető és megfizethető lesz sok alacsony közepes jövedelmű országban, a Közel-Keleten, Afrikában és Indiában, és fontos hatással lesz sok ember életére ezeken a területeken" - mondta Rondelli. A









-program.jpg)







-test.jpg)
.jpg)