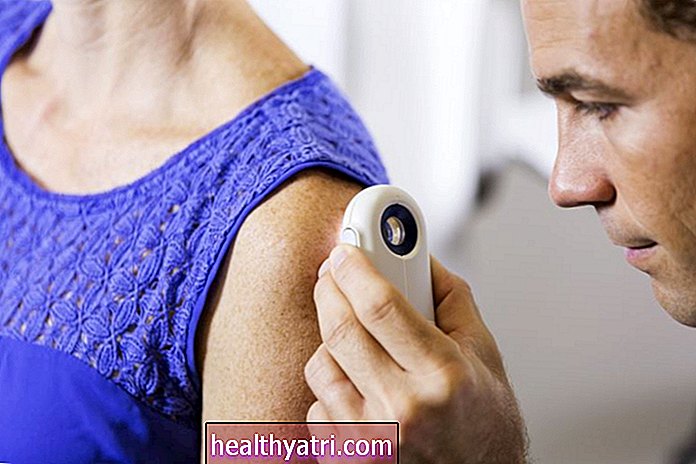
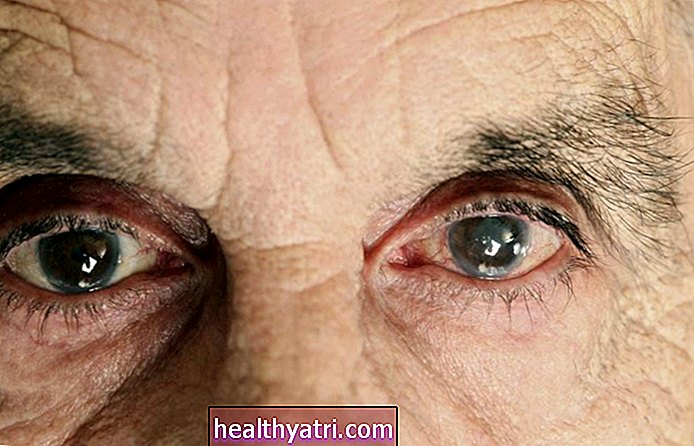
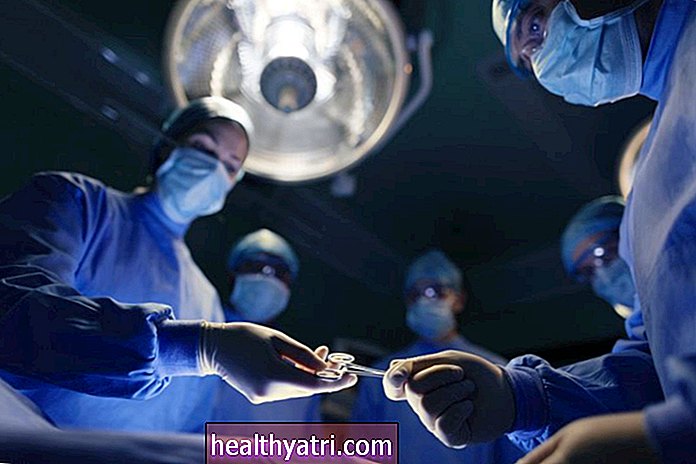
Sasiistock / Getty Images
Key Takeaways
- A Pfizer elnyerte az FDA jóváhagyását a koronavírus elleni vakcina tesztelésének megkezdésére 12 éves és idősebb gyermekeknél.
- Szakértők szerint a gyerekek bevonása a klinikai vizsgálatokba döntő fontosságú egy olyan vakcina kifejlesztése szempontjából, amely megvédi mind a gyermekeket, mind a felnőtteket a COVID-19-től.
- Webhelye szerint a Pfizer már több mint 39 000 önkéntest vett fel tanulmányába. Ezen önkéntesek több mint 34 000-en kaptak már második oltást.
A Pfizer, az egyesült államokbeli gyógyszergyártó cég októberben jelentette be, hogy engedélyt kapott az Egyesült Államok Élelmezési és Gyógyszerügyi Hivatalától (FDA), hogy megkezdhesse 12 éves korú gyermekek bevonását koronavírus elleni vakcinakísérleteibe.
"Ezzel jobban meg fogjuk érteni a vakcina lehetséges biztonságosságát és hatékonyságát több életkorú és háttérrel rendelkező egyéneknél" - áll a társaság frissített közleményében.
Ez lesz az első COVID-19 vakcinakísérlet az Egyesült Államokban, amely gyermekeket is bevon. Októbertől a Pfizer egyike annak a négy amerikai vállalatnak, amelyek vakcinákkal rendelkeznek a 3. fázisú klinikai vizsgálatokban.
A Pfizer már kiterjesztette a vizsgálat 3. fázisát 16 éves és idősebb gyermekekkel, valamint krónikus, stabil humán immunhiányos vírusban (HIV), hepatitis C-ben és Hepatitis B-ben szenvedőkkel.
Miért kell tesztelni a COVID-19 vakcinát gyermekeknél?
Mielőtt a Pfizer megszerezte a jóváhagyást a gyermekek tesztelésének megkezdésére, a szakértők jelentést tettek közzé a folyóiratbanKlinikai fertőző betegségekmegállapítva az ilyen tesztek fontosságát.
"A COVID-19 közvetlen hatása a gyermekekre nagyobb, mint számos más kórokozó esetében, amelyekre ma már hatékony gyermekgyógyászati oltóanyagokkal rendelkezünk" - jegyzi meg a jelentés. „Ezenkívül egyértelműen alulértékelték a gyermekek szerepét a SARS-CoV-2 átvitelében. A gondosan lefolytatott, 2. fázisú klinikai vizsgálatok megfelelő módon kezelhetik a COVID-19 vakcinával kapcsolatos esetleges biztonsági problémákat. ”
Suzanne Pham, orvos
Csak akkor tudjuk legyőzni a vírus terjedését, ha be nem oltjuk gyermekeinket.
- Suzanne Pham, orvosSharon Nachman, a New York-i Stony Brook Gyermekkórház gyermekgyógyászati fertőző betegségek osztályának vezetője egyetért a jelentéssel, elmondva Verywellnek, hogy „a gyermekorvosokat nagyon érdekli a tanulmány részleteinek megismerése és az oltás miként fog működni a gyermekeknél. . ”
Nachman szerint sajátos előnyei vannak az oltás gyermekek tesztelésének. A kutatók képesek lesznek felmérni a rövid és hosszú távú immunválaszt, ideértve azt is, hogy kiderítsék, szükséges-e a felnőtteknél alkalmazott vakcina dózis a gyermekek számára, vagy hasonló immunválaszuk lenne-e az alacsonyabb dózissal szemben.
Nachman szerint azt is fontos megjegyezni, hogy mivel a felnőttek koronavírusát megelőzheti a gyermekek tünetmentes fertőzésének való kitettsége, az egész család kezelésére szolgáló oltóanyag létrehozása „nagy utat jelenthet az otthon és a közösségben történő átvitel csökkentése érdekében”.
Suzanne Pham, MD, a chicagói Weiss Emlékkórház főorvos-helyettese elmondja Verywellnek, hogy minél előbb oltják be a gyerekeket, annál hamarabb csökken az átviteli sebesség.
"A gyermekek hatékony beoltásával csökken a kockázat, hogy a gyermekek a közösségben továbbterjesztik a vírust, különösen azoknál a magas kockázatú embereknél, akik hajlamosabbak súlyos vagy kritikus betegségekre" - mondja Pham Verywellnek. „Ez lehetővé teszi az iskolák számára az újbóli megnyitást, és gyermekeink fejlődéséhez elengedhetetlen tevékenységek ellenőrzött módon folytatódhatnak. Csak akkor tudjuk legyőzni a vírus terjedését, ha be nem oltjuk gyermekeinket. A társadalomban elegendő immunrendszerrel kell rendelkeznünk ahhoz, hogy megakadályozzuk a terjedést. ”
COVID-19 vakcinák: Legyen naprakész arról, hogy mely vakcinák állnak rendelkezésre, kik kaphatják és mennyire biztonságosak.
Hogyan kezdődnek az oltási vizsgálatok?
Pham elmagyarázza, hogy egy vakcina teszteléséhez - felnőtteken vagy gyermekeken - a vállalatnak először be kell nyújtania egy új vizsgálati (IND) vizsgálati kérelmet az FDA-hoz.
Az alkalmazás leírja a vakcinát, annak gyártási módját és milyen minőségellenőrzési teszteket kell alkalmazni. Az alkalmazás állatkísérletek adatait is tartalmazza, amelyek igazolják, hogy a vakcina biztonságos az embereken végzett kezdeti vizsgálatokhoz.
Az FDA magyarázata szerint a pályázati folyamatnak több lépése van:
Az új gyógyszer korai preklinikai fejlesztése során a szponzor elsődleges célja annak meghatározása, hogy a termék ésszerűen biztonságos-e az emberben történő kezdeti használatra, és a vegyület olyan farmakológiai aktivitást mutat-e, amely indokolja a kereskedelmi fejlesztést.
Amikor egy terméket életképes jelöltnek találnak a továbbfejlesztésre, a szponzor ezután arra összpontosít, hogy összegyűjtse azokat az adatokat és információkat, amelyek szükségesek annak megállapításához, hogy a termék korlátozott, korai stádiumú klinikai vizsgálatok során nem teszi ki az embereket ésszerűtlen kockázatoknak.
A vakcinát ezután az 1. fázisú vizsgálatoknak vetik alá, amelyek a Pham szerint „biztonsági és immunogenitási vizsgálatok, amelyeket kis számú, szoros megfigyelés alatt álló embernél végeztek”.
"A 2. fázis dózistartomány-vizsgálatokból áll, és nagyobb (száz) emberre terjed ki" - mondja Pham. „Ezután a 3. fázisú kísérletek emberi alanyok ezreit kívánják bevonni a hatékonyság dokumentálása érdekében, és folytatják a biztonsági adatok áttekintését.”
Webhelye szerint a Pfizer több mint 39 000 önkéntest vett fel tanulmányába. Közülük több mint 34 000-en kapták meg az oltás második adagját.
Mit jelent ez az Ön számára
A 3. fázisú klinikai vizsgálat, amely magában foglalja a gyermekek COVID-19 vakcinájának tesztelését, a fejlődés jele. Egy oltást azonban nem lehet siettetni. Az eredmények véglegesítése időbe telik a kísérleti résztvevők, valamint olyan felnőttek és gyermekek biztonságának védelme érdekében, akik végül megkapják az oltás kész verzióját.




.jpg)